Bevezetés
A hátsó reverzibilis encephalopathia szindróma (PRES) a különböző klinikai entitások ritka szövődménye. Előfordulása ismeretlen, széles körben, 14 és 78 év között jelentették, átlagéletkoruk 44 év, a férfi / nő arány 0,8 / 1,1. Bár a prognózis általában kedvező, a halálozási arány legfeljebb 15 % -ról számoltak be.2 Ezt tipikus klinikai – radiológiai megnyilvánulások határozzák meg, általában átmeneti.3 Akut vagy szubakut formában, gyakoriságának csökkenő sorrendjében encephalopathiával, görcsrohamokkal, fejfájással, látászavarokkal és fokális neurológiai deficittel fordul elő.4 Számos kórélettani elméletet posztuláltak, kettő a legelfogadottabb. Az első azt sugallja, hogy a hirtelen vérnyomásnövekedés meghaladja az agyi véráramlás önszabályozását, értágulatot és hiperperfúziót okozva, a vér – agy gát (BBB) megrepedésével és vazogén ödémával.5 Így klasszikusan összefüggésbe hozható eclampsia és hipertóniás encephalopathia; azonban a betegek 20–30% -a normotenzív, ami a gyulladásos mediátorok által okozott közvetlen endoteliális toxicitás második elméletét sugallja, amely jobban összefügg az immunszuppresszív kezeléssel, veseelégtelenséggel, kötőszöveti rendellenességekkel vagy szepszissel járó betegekkel. Az agy MR-vizsgálata meghatározó a diagnózis szempontjából, amely vazogén ödémát mutat, általában a hátsó agyi területen, kétoldali és szimmetrikus. 8 Mivel a PRES diagnózisa magas klinikai és képi gyanút igényel, a későbbi korai kezelés megteremtésével prognózis; A munka célja információk nyújtása az SLE-hez kapcsolódó szokatlan szindróma felismerésére és kezelésére.
Az eset leírása
Egy 25 éves mestizo nő, Quito-ból (Ecuador), személyi patológiával. a hypothyreosis és az SLE előzményei, amelyeket 2012 decemberében diagnosztizáltak, 21 éves korukban. 2016 decemberében, 4 évvel az SLE diagnózisa után, akut hasmenéses betegség által kiváltott súlyosbodást mutatott be; izom-csontrendszeri (ízületi gyulladás, myalgias) és mucocutan (szájüregi fekélyek) megnyilvánulásokkal, szerositis (jobb oldali pleurális folyadékgyülem), bicytopenia (vérszegénység, thrombocytopenia), veseelégtelenség (hematuria, proteinuria, akut veseelégtelenség, III. heveny akut veseelégtelenség besorolása) és artériás hipertónia esetén (AHT); mindez magas SLEDAI értéket adott neki (értéke: 23). A vese biopsziában II fokozatú fokális proliferatív lupus glomerulonephritisről számoltak be, amely nem felel meg intenzív lupus aktivitással; az antifoszfolipid szindrómának tulajdonítható változások, valamint ezen antitestek negativitása nélkül. A többszerves részvétel miatt 1 g metilprednizolont kapott intravénásan 3 napig, vérkészítmények pótlását, 6 plazmaferezis, hemodyalisis, napi 10 mg amlodipin, 50 mg / nap atenolol és 1 g / 12 óra mikofenolát mofetil szájon át, mivel emésztőrendszeri intoleranciát mutatott be nagyobb dózisokkal szemben. Három héttel a felvétel után elfogadható analitikai és klinikai javulást mutatott a kezelés során, ezért kórházi mentességét jelezték. Huszonnégy órával később a páciens görcsös állapotban tér vissza. Sürgősségi esetekben megkezdték a légutak kezelését, intravénás görcsoldókat 10 mg diazepámmal, 3 mg midazolámmal, 1 g fenitoinral és az intenzív osztályra vitték.
Cranialis tomográfiát kértek, amely nem mutatott ischaemia vagy vérzés jeleit. ; tömeges hatás nélküli jobb oldali occipitalis hypodensitást figyeltek meg, és emiatt kibővítették a vizsgák sorrendjét annak etiológiájának azonosítására. A metabolikus, fertőző és farmakológiai okokat kizárták. A nehezen kontrollálható AHT miatt (190/100 Hgmm-ig 130 mmHg-os átlagos artériás nyomással) a betegnek legfeljebb 6 vérnyomáscsökkentő gyógyszerre volt szüksége; atenolol 50mg / 12h, losartan 100mg / nap, amlodipin 10mg / nap, doxazosin 2mg / 6h nasogastricus csövön keresztül, intravénásan beadott nitroprussid 50mg / nap és furosemid 20mg / 6h. A súlyos lupus aktivitás (SLEDAI 21: rohamok, hematuria, proteinuria, hypocomplementemia, anti-DNS, trombocitopénia) miatt ismét metilprednizolonnal kezelték 1g / 3 nap alatt. Az elektroencefalogram nem mutatott epileptiform aktivitást. Olyan agyi angiorezonanciát kértek tőle, amelyben nem találtak vaszkulitisznek vagy a központi idegrendszer trombózisának megfelelő eredményeket. Az agy MR-vizsgálata tipikus PRES-képeket mutatott (1. ábra), amelyek kialakulása összefüggésben lenne az exacerbált SLE-vel, súlyos AHT-vel, lupus glomerulonephritisrel és immunszuppresszánsok alkalmazásával, így orális 60 mg / 6 órás nimodipint adtak hozzá, és a kiváltó tényezőket kontrollálták .A kábítószer által kiváltott lupus kockázata miatt a fenitoint fokozatosan kivonták, a levetiracetam fokozatos emelkedésével a nasogastricus csövön keresztül 1g / 12h-ig. Az 1. táblázat részletezi a vonatkozó kiegészítő vizsgálatokat. A nyomon követés során nem mutatott új görcsös eseményeket, a vesefunkció helyben maradt, a vérnyomásértékek javultak (MAP 85–90mmHg) és a lupus aktivitása csökkent (SLEDAI 13: hematuria, proteinuria, hypocomplementemia, anti-DNS , thrombocytopenia). A kontroll agy MRI-je a korábbi elváltozások involzióját bizonyította (2. ábra).
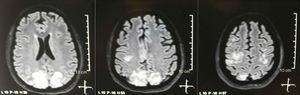
Az agy egyszerű + diffúziós magmágneses rezonancia képalkotása felvételkor: bilaterális, szimmetrikus, hiperintenzív elváltozások FLAIR-szekvenciában az occipitalis és a parietalis lebeny fehérállományában.
Az eset releváns kiegészítő tanulmányai.
| Dátum | Klinikai vizsgálatok |
|---|---|
| Az SLE súlyosbodása 4 év diagnózis után | HB: hemoglobin 7mg / dl; hematokrit 22,2%; vérlemezkék 75 000 / μlC-reaktív fehérje: 2,52 mg / dl; prokalcitonin 0,348 ng / ml, kreatinin 5,7 mg / dl (eGFR CKD-EPI: 9,6 ml / perc / 1,73 m2); karbamid 187mg / dlKreatin-kináz: 18U / l; laktát-dehidrogenáz: 237U / lMU: fehérjék 150mg / dl; vörösvértestek 40,8 / mező; proteinuria: 1452mg / 24hC3: 36mg / dl; C4: 15 mg / dl; anti-dsDNS: 200 NE / ml Lupus antikoaguláns, anticardiolipinek, béta 2-glikoprotein 1: negatív Vese biopszia; fokális lupus proliferatív II. osztályú glomerulonephritis (ISN / RPS), krónikus és aktivitási indexe 4 |
| Visszafogás | HB: hemoglobin 8,90mg / dl; hematokrit 26,3%; vérlemezkék 130 000 / μl; kreatinin 2,77 mg / dl (eGFR CKD-EPI: 22,8 ml / perc / 1,73 m2); karbamid 105,1 mg / dl Laktát-dehidrogenáz: 527U / l; y-glutamil-transzferáz 79U / l; lúgos foszfatáz: 138U / l; teljes bilirubin: 1,23 mg / dl; közvetlen: 0,50 mg / dl; közvetett: 0,73 mg / dlMU: fehérjék 300 mg / dl; vörösvértestek 44 / mező; proteinuria 1974mg / 24h Egyszerű koponyatomográfia: jobb oldali occipitalis hypodensity, tömeghatás nélkül Ischaemia vagy vérzés jelei nincsenek Elektroencefalogram: agyi aktivitás 4Hz-en alacsony feszültségű theta ritmusban. Csúcs éles hullámok jelenléte hátsó delta ritmusokkal, interhemisphericus szimmetriával, paroxizmális epileptiform aktivitás nélkülAz agy mágneses rezonancia angiográfiája artériás és vénás fázisokban: vaszkuláris elváltozások nélkül > |
anti-dsDNS: anti-kettős szálú DNS; HB: hematikus biometria; MU: mikroszkopikus vizeletvizsgálat; ISN / RPS: Nemzetközi Nefrológiai Társaság / Vese Patológiai Társaság; SLE: szisztémás lupus erythematosus; eGFR CKD-EPI: a krónikus vesebetegség-epidemiológia együttműködés egyenletének felhasználásával becsült glomeruláris szűrési ráta. / div>
Megbeszélés
A PRES első leírása óta, amelyet 1996-ban Hinchey és munkatársai készítettek, ennek az entitásnak több aspektusa ismerete bővült. A reverzibilis posterior leukoencephalopathia szindróma eredeti neve nem megfelelő, mivel a képalkotó változások nem mindig korlátozódnak az agy fehérállományára és klinikai megnyilvánulásai nem mindig visszafordíthatók.9 Az első 15 jelentett eset hipertóniás encephalopathiában, eklampsiában vagy immunszuppresszív betegeknél fordult elő kezelés.10 Más entitások szövődményeként is megfigyelték, például szepszis, veseelégtelenség és kötőszöveti rendellenességek; ezért jelenleg ismert, hogy az endothel diszfunkciót okozó kockázati tényezők kulcsfontosságúak a PRES kialakulásához.11 A globális incidencia nem ismert, de a retrospektív vizsgálatok adatai azt mutatják, hogy gyakoribb 39 és 47 év közötti egyéneknél, általában nők, társbetegségekkel, például hipertóniás, vese- vagy autoimmun rendellenességekkel.12 SLE-ben szenvedő betegeknél számos autoantitest irányul az endothelium ellen; aktiválása, a tapadási molekulák (E-szelektin, VCAM-1, ICAM-1) expressziója és gyulladásgátló citokinek, például IL-1β, TNFα és IL-6 expozíciója, ami a BBB megzavarását és neurológiai szövődmények megjelenését okozza.13 Beszámoltak arról, hogy az SLE-vel diagnosztizált embereknél a PRES mérsékelt vagy súlyos lupus aktivitással összefüggésben fordul elő, valamint veseelégtelenséggel és rosszul kontrollált magas vérnyomással jár.14
A PRES klinikai megnyilvánulásait tekintve változó fokú encephalopathia jellemzi, a zavartságtól a stuporig (50–80%), görcsrohamok (60–75%), fejfájás (50%) és látászavarok a homályos látástól a kortikális vakságig (33%); szokatlan a fokális neurológiai hiány (10–15%) és az epilepsziás állapot (5–15%) .15 E betegek neurológiai kompromisszumának kezdeti értékeléséhez általában koponyaűri számított axiális tomográfia (CT) vizsgálatát kérik, gyakran normális, vagy kortikális – subcorticalis hypodensitásokat mutat, főleg a hátsó agyi régiókban.16 Az agy MR-vizsgálata meghatározza a diagnózist, amely vazogén ödémát mutat, általában az occipitalis és a parietalis lebeny fehérállományában (a hátsó agyi keringés területén). , hiperintenzív elváltozásokként vizualizálva a T2-ben és a FLAIR-ben, kétoldalúak és szimmetrikusak.17 A fehérállomány preferenciális szerepvállalása myelinizált rostok, arteriolák és kapillárisok szerkezetéből adódik, ami nagyobb lazaságot kölcsönöz neki. Hasonlóképpen, az elülső agyi keringés edényei, amelyeknek nagyobb a szimpatikus beidegződésük, vazokonstrikcióval képesek megfelelően reagálni a magas vérnyomás miatt másodlagos agyi véráramlás hirtelen növekedésére; a vertebrobasilaris rendszerben kevésbé fejlett védőmechanizmus.18 Ritkábban a szürkeállomány és más lebenyek érintettek lehetnek. A diffúziós szekvenciával készült képek lehetővé teszik a PRES-re jellemző vazogén ödéma és az atipikusan előforduló és infarktusig terjedő citotoxikus ödéma megkülönböztetését. fókuszos éles hullámok jelenléte. A PRES-hez kapcsolódó rohamokban szenvedő betegeknél a fő elektroencefalográfiai változás a theta / delta frekvenciák általános lassulása. 20 A cerebrospinális folyadék elemzése olyan nem specifikus változásokat mutat, mint például a sejtek és a fehérjék enyhe növekedése, ezért hasznos, amikor kényelmes a központi idegrendszeri fertőzés kizárására.21 A fent említett teszteken kívül azokat, amelyeket szükségesnek tartanak a differenciáldiagnózishoz, főként neurolupus, metabolikus és parainfektikus encephalopathia, encephalitis, a hátsó agyi artéria infarktusa és demyelinizációs rendellenességek esetén kell végrehajtani.22,23 A fentiek alapján a 3. ábra mutatja a Fugate és mtsai által javasolt algoritmust. a PRES diagnosztizálására, amelynek célja még az atipikus esetek azonosítása is.
Diagnosztikai algoritmus a hátsó reverzibilis encephalopathia szindrómához.
Betegünknél a klinikai megjelenést, a többszörös kockázati tényezőket, képalkotó eredményeket és egyéb etiológiák kizárását figyelembe véve a PRES diagnózisa következtetett. A görcsoldó gyógyszerrel és az agyi ödémával való tüneti kezelést időben indították el, az okozó tényezők ellenőrzésével együtt: súlyos magas vérnyomás, súlyos aktivitású SLE, lupus glomerulonephritis, immunszuppresszív gyógyszerek; a diagnózis megerősítése a nyomon követés során a klinikai és képi változások megoldásával. A PRES kezelése tekintetében csökkenteni kell a vérnyomást, kezelni kell a rohamokat és ellenőrizni kell a kiváltó okot. A gyors vérnyomáscsökkenés agyi iszkémiát okozhat, ezért javasolják az átlagos vérnyomás elérését 105 és 125 Hgmm között, anélkül, hogy az első órában meghaladná ennek a csökkenésnek a 25% -át. Az első vonalbeli gyógyszerek a kalciumcsatorna-blokkolók (a választott nicardipin vagy a nimodipin, amely megakadályozza az agyi érgörcsöt is) vagy a béta-blokkolók (például a labetalol). A nátrium-nitroprusszid vagy a hidralazin másodlagos gyógyszerként alkalmazható. A nitroglicerint értágító hatása miatt kerülni kell, ami növelné az agyi ödémát.24 A rohamok kezelése hasonló a többi epilepsziás roham kezeléséhez. Benzodiazepineket, például lorazepamot vagy diazepamot alkalmaznak első vonalbeli terápiaként. Második vonalként fenitoin vagy valproát, különösen status epilepticus vagy fenobarbitál esetén. A magnézium-szulfát terhes nőknél alkalmazható. Refrakter rohamokban propofol o pentobarbitalt adhatunk.25 SLE-ben szenvedő betegeknél kerülni kell azokat a gyógyszereket, amelyek gyógyszer által kiváltott lupust okozhatnak, mint például a hidralazin, metildopa, kaptopril, fenitoin, valproát és karbamazepin. Viták vannak az immunszuppresszív gyógyszerek kezelésével kapcsolatban a PRES kezelésében SLE-ben szenvedő betegeknél. 26 A PRES megoldása után a rohamok ritkák, és ezért mérlegelni kell a görcsoldók abbahagyását, amíg megfelelő kontroll fennáll. a kockázati tényezők.Időszerű és megfelelő kezeléssel a PRES-ben szenvedő betegek többsége kielégítően fejlődik a tünetek remissziójával és a képi elváltozásokkal néhány nap vagy hét alatt, bár az esetek 9–33% -ában speciálisan vérzéses szövődményeket figyeltek meg, így ez az eset rávilágít felismerésének és kezelésének fontosságára, ami gyakran kihívást jelent. 28
Következtetések
A PRES diagnózisa magas klinikai és képi gyanút igényel. A tünetek és a kiváltó ok ellenőrzésével történő időben történő kezelés megerősíti a diagnózist a nyomon követés során, a klinikai és képi változások megoldásával; ellenkező esetben neurológiai következményeket vagy halált okozhat.
Érdekkonfliktus
A szerzők kijelentik, hogy nincsenek összeférhetetlenségük.