Úvod
Syndrom zadní reverzibilní encefalopatie (PRES) je vzácnou komplikací různých klinických entit. Jeho výskyt není znám, protože byl hlášen v širokém rozmezí věků od 14 do 78 let, s průměrným věkem 44 let a poměrem mužů a žen 0,8 / 1,1 Přestože prognóza je obvykle příznivá, úmrtnost až 15 Bylo hlášeno%. 2 Je určováno typickými klinicko-radiologickými projevy, obvykle přechodnými.3 Buď v akutní nebo subakutní formě, v sestupném pořadí podle frekvence se vyskytuje u encefalopatie, záchvatů, bolestí hlavy, poruch zraku a fokálního neurologického deficitu.4 Bylo postulováno několik patofyziologických teorií, z nichž dvě jsou nejvíce přijímány. První naznačuje, že náhlé zvýšení krevního tlaku převyšuje samoregulaci průtoku krve mozkem, což způsobuje vazodilataci a hyperperfuzi s prasknutím hematoencefalické bariéry (BBB) a vazogenním edémem.5 Bylo tedy klasicky spojeno s eklampsie a hypertenzní encefalopatie; 20–30% pacientů je však normotenzních, což naznačuje druhou teorii přímé endoteliální toxicity způsobené zánětlivými mediátory, která více souvisí s pacienty s imunosupresivní léčbou, selháním ledvin, poruchami pojivové tkáně nebo sepse.6 Vyskytuje se u 7 magnetické rezonance ( Pro diagnostiku je určující MRI) mozku, který vykazuje vazogenní edém, obvykle na zadním mozkovém území, bilaterální a symetrický.8 Jelikož diagnóza PRES vyžaduje vysoké klinické a zobrazovací podezření, s následným zavedením včasné léčby pro prognóza; cílem této práce je poskytnout informace pro rozpoznání a zvládnutí tohoto neobvyklého syndromu spojeného se SLE.
Popis případu
25letá mestická žena z Ekvádoru v Quitu s osobními patologickými příznaky předchůdci hypotyreózy a SLE, diagnostikováni v prosinci 2012, ve věku 21 let. V prosinci 2016, 4 roky po diagnóze SLE, představila exacerbaci vyvolanou akutním průjmovým onemocněním; s muskuloskeletálními (artritida, myalgie) a mukokutánními (vředy v ústech) projevy, serositis (pravý pleurální výpotek), bicyktopenie (anémie, trombocytopenie), postižení ledvin (hematurie, proteinurie, akutní selhání ledvin, klasifikace sítě pro akutní poškození ledvin III) a arteriální hypertenze (AHT); to vše jí poskytlo vysoký SLEDAI (hodnota: 23). Renální biopsie zaznamenala fokální proliferativní lupus glomerulonefritidu třídy II, což neodpovídá intenzivní aktivitě lupusu; bez změn způsobených antifosfolipidovým syndromem, stejně jako negativita těchto protilátek. Vzhledem k multiorgánovému postižení dostávala pulsy 1 g methylprednisolonu intravenózně po dobu 3 dnů, výměnu krevních produktů, 6 sezení plazmaferézou, hemodyalisou, amlodipin 10 mg / den, atenolol 50 mg / den a mykofenolát mofetil 1 g / 12 h perorálně, protože vykazovala gastrointestinální intoleranci na vyšší dávky. Tři týdny po přijetí představila přijatelné analytické a klinické zlepšení léčby, a proto bylo indikováno její propuštění z nemocnice. O dvacet čtyři hodin později pacient znovu vstoupil s křečovitým stavem. V naléhavých případech zahájili řízení dýchacích cest, intravenózní antikonvulziva s diazepamem 10 mg, midazolamem 3 mg, fenytoinem 1 g a převedli ji na jednotku intenzivní péče.
Byla požadována kraniální tomografie, která nevykazovala známky ischemie nebo krvácení ; byla pozorována pravá týlní hypodenzita bez hromadného účinku a z tohoto důvodu bylo rozšířeno pořadí zkoušek, aby se určila její etiologie. Metabolické, infekční a farmakologické příčiny byly vyloučeny. Vzhledem k obtížně kontrolovatelné AHT (až 190/100 mmHg se středním arteriálním tlakem 130 mmHg) pacient potřeboval až 6 antihypertenziv; atenolol 50mg / 12h, losartan 100mg / den, amlodipin 10mg / den, doxazosin 2mg / 6h nasogastrickou sondou a nitrožilní nitroprusid 50mg / den a furosemid 20mg / 6h. Kvůli závažné aktivitě lupusu (SLEDAI 21: záchvaty, hematurie, proteinurie, hypokomplementemie, anti-DNA, trombocytopenie) byla znovu léčena methylprednisolonem 1 g / 3 dny. Elektroencefalogram nevykazoval epileptiformní aktivitu. Bylo požadováno, aby mozková angioresonance nebyla nalezena v souladu s vaskulitidou nebo trombózou centrálního nervového systému. MRI mozku ukázalo typické obrazy PRES (obr. 1), jejichž vývoj by souvisel s exacerbovaným SLE, těžkou AHT, lupus glomerulonefritidou a užíváním imunosupresiv, takže byl přidán perorální nimodipin 60mg / 6h a byly kontrolovány spouštěcí faktory .Kvůli riziku lupusu vyvolaného léky byl fenytoin postupně vysazován s postupným zvyšováním levetiracetamu až na 1 g / 12 h nasogastrickou sondou. Tabulka 1 podrobně popisuje příslušné doplňkové studie. Během sledování neprokázala nové křečové příhody, funkce ledvin zůstala stacionární, hodnoty krevního tlaku se zlepšily (MAP 85–90 mmHg) a aktivita lupusu se snížila (SLEDAI 13: hematurie, proteinurie, hypocomplementemie, anti-DNA , trombocytopenie). MRI mozku kontroly prokázalo involuci předchozích lézí (obr. 2).
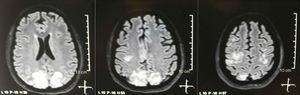
Jednoduché + difúzní zobrazování nukleární magnetickou rezonancí mozku při vstupu: bilaterální, symetrické, hyperintenzivní léze v sekvenci FLAIR v bílé hmotě okcipitálních a parietálních laloků.
Relevantní doplňkové studie případu.
| datum | Klinické testy |
|---|---|
| Exacerbace SLE 4 roky po diagnóze | HB: hemoglobin 7mg / dl; hematokrit 22,2%; destičky 75 000 / μlC-reaktivní protein: 2,52 mg / dl; prokalcitonin 0,348 ng / ml Kreatinin 5,7 mg / dl (eGFR CKD-EPI: 9,6 ml / min / 1,73 m2); močovina 187 mg / dl Kreatin kináza: 18U / l; laktátdehydrogenáza: 237U / lMU: proteiny 150mg / dl; červené krvinky 40,8 / pole; proteinurie: 1452mg / 24hC3: 36mg / dl; C4: 15 mg / dl; anti-dsDNA: 200 IU / ml Lupus antikoagulant, antikardiolipiny, beta 2-glykoprotein 1: negativní Biopsie ledvin; fokální lupus proliferativní glomerulonefritida třídy II (ISN / RPS) s indexem chroničnosti a aktivity 4 |
| Readmise | HB: hemoglobin 8,90 mg / dl; hematokrit 26,3%; krevní destičky 130 000 / μl, kreatinin 2,77 mg / dl (eGFR CKD-EPI: 22,8 ml / min / 1,73 m2); močovina 105,1 mg / dlLaktátdehydrogenáza: 527U / l; y-glutamyltransferáza 79U / l; alkalická fosfatáza: 138U / l; celkový bilirubin: 1,23 mg / dl; přímé: 0,50 mg / dl; nepřímo: 0,73 mg / dlMU: proteiny 300mg / dl; červené krvinky 44 / pole; proteinurie 1974mg / 24hJednoduchá lebeční tomografie: pravá týlní hypodenzita, bez hromadného účinku. Žádné známky ischemie nebo krvácení Elektroencefalogram: aktivita mozku na pozadí při 4 Hz v nízkém napětí theta rytmu. Přítomnost vrcholných ostrých vln s rytmy zadní delty s interhemisférickou symetrií, bez paroxysmální epileptiformní aktivity Magnetická rezonanční angiografie mozku v arteriálních a žilních fázích: bez vaskulárních alterací |
Anti-dsDNA: anti-dvouvláknová DNA; HB: hematická biometrie; MU: mikroskopická analýza moči; ISN / RPS: Mezinárodní nefrologická společnost / Společnost pro renální patologii; SLE: systémový lupus erythematodes; eGFR CKD-EPI: rychlost glomerulární filtrace odhadovaná pomocí rovnice spolupráce s chronickými onemocněními ledvin a epidemiologií.
Diskuse
Od prvního popisu PRES, který provedli v roce 1996 Hinchey a kol., se rozšířila znalost několika aspektů této entity. Jeho původní název syndromu reverzibilní zadní leukoencefalopatie byl nevhodný, protože zobrazovací změny nejsou vždy omezeny na bílou hmotu mozku a jeho klinické projevy nejsou vždy reverzibilní.9 Prvních 15 hlášených případů se vyskytlo u pacientů s hypertenzní encefalopatií, eklampsií nebo u pacientů s imunosupresivní léčbou léčba.10 Bylo také pozorováno jako komplikace jiných entit, jako je sepse, selhání ledvin a poruchy pojivové tkáně; proto je v současné době známo, že rizikové faktory, které způsobují endoteliální dysfunkci, jsou pro rozvoj PRES klíčové.11 Globální výskyt není znám, ale údaje retrospektivních studií naznačují, že je častější u jedinců mezi 39 a 47 lety, obvykle ženy s komorbiditami, jako jsou hypertenzní, renální nebo autoimunitní poruchy.12 U pacientů se SLE je mnoho autoprotilátek namířeno proti endotelu; produkující jeho aktivaci, expresi adhezních molekul (E-selektin, VCAM-1, ICAM-1) a expozici prozánětlivým cytokinům, jako jsou IL-1β, TNFα a IL-6, což způsobuje narušení BBB a výskyt neurologických komplikací. Bylo hlášeno, že u lidí s diagnostikovanou SLE se PRES vyskytuje v souvislosti se středně těžkou až těžkou aktivitou lupusu, stejně jako v souvislosti se selháním ledvin a špatně kontrolovanou hypertenzí.14
Pokud jde o klinické projevy PRES, je charakterizován proměnlivým stupněm encefalopatie, od zmatenosti po stupor (50–80%), záchvaty (60–75%), bolesti hlavy (50%) a poruchy vidění od rozmazaného vidění po kortikální slepotu (33%); neobvyklý je fokální neurologický deficit (10–15%) a stav epileptický (5–15%) .15 Pro počáteční posouzení neurologického kompromisu u těchto pacientů je obvykle vyžadováno skenování kraniální počítačovou axiální tomografií (CT), které je často normální nebo může vykazovat kortikálně-subkortikální hypodensity, převážně v zadních oblastech mozku.16 MRI mozku určuje diagnózu a vykazuje vazogenní edém, obvykle v bílé hmotě okcipitálního a temenního laloku (území zadního mozkového oběhu) , vizualizované jako hyperintenzivní léze v T2 a FLAIR, dvoustranné a symetrické.17 Přednostní zapojení bílé hmoty je způsobeno strukturou myelinizovaných vláken, arteriol a kapilár, které jí propůjčují větší laxnost. Podobně cévy přední mozkové cirkulace, které mají větší sympatickou inervaci, mohou adekvátně reagovat vazokonstrikcí na náhlé zvýšení průtoku krve mozkem sekundárně po hypertenzi; ochranný mechanismus méně vyvinutý ve vertebrobazilárním systému.18 Méně často může být ovlivněna šedá hmota a další laloky. Snímky s difuzními sekvencemi umožňují rozlišovat mezi vasogenním edémem typickým pro PRES a cytotoxickým edémem, který se může vyskytovat atypicky a může vést k infarktu.19 Elektroencefalogram nekoreluje vždy s neurologickým postižením, ale může odhalit encefalopatii přítomnost ostrých ostrých vln. U pacientů se záchvaty spojenými s PRES je hlavní elektroencefalografickou změnou obecné zpomalení frekvencí theta / delta.20 Analýza mozkomíšního moku ukazuje nespecifické změny, jako je mírné zvýšení celulárnosti a proteinů, a proto je užitečné, když je vhodné k vyloučení infekce v centrálním nervovém systému.21 Kromě výše zmíněných testů jsou považovány za nezbytné pro diferenciální diagnostiku, zejména s neurolupem, metabolickou a parainfekční encefalopatií, encefalitidou, infarktem zadní mozkové tepny a demyelinizačními poruchami. musí být provedeno.22,23 Na základě výše uvedeného ukazuje obr. 3 algoritmus navržený Fugate et al. pro diagnostiku PRES, jejímž cílem je identifikovat i atypické případy.15
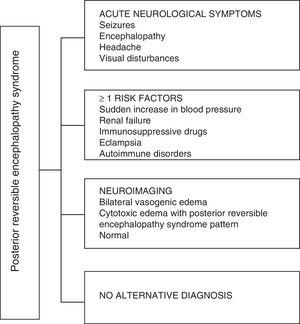
Diagnostický algoritmus pro syndrom zadní reverzibilní encefalopatie.
U našeho pacienta byla diagnóza PRES s ohledem na klinický obraz spolu s mnoha rizikovými faktory, zobrazovacími nálezy a vyloučením jiných etiologií uzavřeno. Symptomatická léčba antikonvulzivy a anti-cerebrální edém byla zahájena včas, spolu s kontrolou příčinných faktorů: těžká hypertenze, SLE s těžkou aktivitou, lupus glomerulonefritida, imunosupresivní léky; ratifikace diagnózy během sledování s vyřešením klinických a zobrazovacích změn. Pokud jde o léčbu PRES, měl by se snížit krevní tlak, léčit záchvaty a kontrolovat spouštěč. Rychlé snížení krevního tlaku by mohlo způsobit mozkovou ischemii, a proto se navrhuje cíl průměrného krevního tlaku mezi 105 a 125 mmHg, aniž by během první hodiny došlo k překročení 25% tohoto snížení. Léky první volby jsou blokátory kalciových kanálů (nikardipin nebo nimodipin podle volby, které rovněž zabraňují mozkovému vazospazmu) nebo betablokátory (například labetalol). Jako léky druhé linie lze použít nitroprusid sodný nebo hydralazin. Nitroglycerinu je třeba se vyhnout kvůli jeho vazodilatačnímu účinku, který by zvýšil mozkový edém.24 Léčba záchvatů je podobná jako u jiných epileptických záchvatů. Jako léčba první linie se používají benzodiazepiny, jako je lorazepam nebo diazepam. Jako druhá linie, fenytoin nebo valproát, zejména u status epilepticus, nebo fenobarbital. Síran hořečnatý lze použít u těhotných žen. U refrakterních záchvatů můžeme podávat propofol-pentobarbital.25 U pacientů se SLE je třeba se vyhnout lékům, které by mohly způsobit lupus vyvolaný léky, jako je hydralazin, methyldopa, captopril, fenytoin, valproát a karbamazepin. O léčbě imunosupresivními léky při léčbě PRES u pacientů se SLE se vedou polemiky.26 Po vyřešení PRES jsou záchvaty časté, a proto je třeba uvažovat o vysazení antikonvulziv, pokud je adekvátní kontrola rizikové faktory.27 Při včasné a adekvátní léčbě se většina pacientů s PRES vyvíjí uspokojivě s ústupem symptomů a zobrazovacích lézí během několika dní nebo týdnů, ačkoli u 9–33% případů byly pozorovány komplikace, zvláště hemoragické. případ zdůrazňuje důležitost jeho uznání a řízení, což je často výzva.28
Závěry
Diagnóza PRES vyžaduje vysoké klinické a zobrazovací podezření. Včasná léčba s kontrolou symptomů a základní příčiny ratifikuje diagnózu během sledování s vyřešením klinických a zobrazovacích změn; jinak by to mohlo způsobit neurologické následky nebo smrt.
Střet zájmů
Autoři prohlašují, že nedochází ke střetu zájmů.