Vattens ytspänning är cirka 72 mN / m vid rumstemperatur, vilket är en av de högsta ytspänningarna för vätska. Det finns bara en vätska med högre ytspänning och det är kvicksilver som är en flytande metall med ytspänningen på nästan 500 mN / m. Varför kvicksilvers ytspänning är så hög kommer också att framgå efter att ha läst det här korta blogginlägget.
Den höga ytspänningen hos vatten orsakas av starka molekylära interaktioner till sammanhängande interaktioner mellan molekylerna i vätskan. I huvuddelen av vätskan har molekylerna närliggande molekyler på varje sida. Molekyler drar varandra lika i alla riktningar och orsakar en nettokraft på noll. Vid gränssnittet har emellertid de flytande molekylerna endast hälften av de angränsande flytande molekylerna jämfört med huvuddelen av vätskan. Detta gör att molekylen associeras starkare med molekylerna vid dess sidor och orsakar en netto inåtgående kraft mot vätskan. Denna kraft motstår ytbrottet och kallas ytspänning.
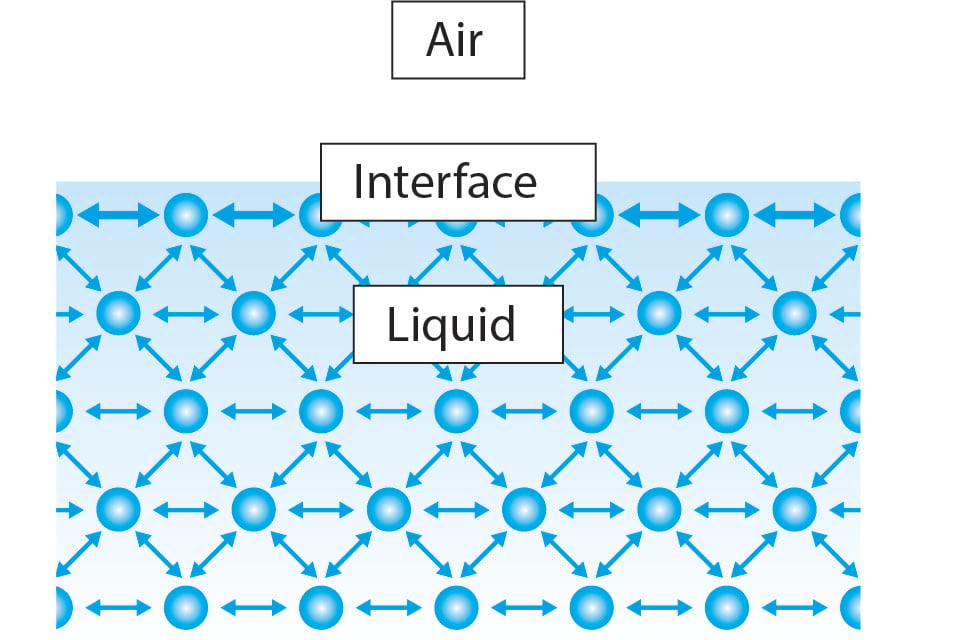
Med denna förklaring i åtanke är det då klart att alla vätskor kommer att ha samma egenskaper men varför vattens ytspänning är mycket högre än till exempel etanol.
För att förstå detta måste vi tänka på bindningarna mellan molekylerna. Som förklarats orsakar den sammanhängande kraften mellan molekylerna ytspänningar. Ju starkare den sammanhängande kraften, desto starkare är ytspänningen. Vattenmolekylen har två väteatomer bundna till en syreatom genom kovalent bindning. På grund av den höga elektronegativiteten hos syre kommer den att ha en stor del av den negativa laddningen på sin sida medan väte kommer att vara mer positivt laddat. Detta orsakar en elektrostatisk attraktion mellan väteatomen i en molekyl och syreatomen i en annan. Formade bindningar kallas vätebindningar som leder till starka sammanhängande krafter mellan vattenmolekylerna och hög ytspänning av vatten.
Som nämnts i början av bloggen förklarar detta också varför kvicksilver har så hög ytspänning. Eftersom kvicksilver är en metall är bindningarna mellan molekylerna metallbindningar som är mycket starkare än vätebindningarna vilket leder till mycket höga sammanhängande krafter och hög ytspänning.
Att lära sig mer om vikten av ytspänning genom länken nedan
