Redaktörens anmärkning: Kommentar baserad på Wilson DP, Jacobson TA, Jones PH, et al. Användning av lipoprotein (a) i klinisk praxis: en biomarkör vars tid har kommit. Ett vetenskapligt uttalande från National Lipid Association. J Clin Lipidol 2019; 13: 374-92.
Inledning
Den traditionella lipidprofilen har tjänat som en grundpelare i riskbedömning av aterosklerotisk hjärt-kärlsjukdom (ASCVD) i årtionden. Detta verktyg blev ännu viktigare när riktade terapier, såsom statiner och nyligen ezetimib- och proproteinkonvertas-subtilisin / kexin typ 9 (PCSK9) -hämmare, blev tillgängliga. Även med dessa framsteg inom lipidhantering, och mer allmänt i riktning mot traditionella kardiovaskulära riskfaktorer, pekar pågående risk hos många patienter på ett behov av att undersöka andra bidragsgivare som möjliga terapeutiska mål. Lipoprotein (a) (Lp) är en lovande biomarkör för att hjälpa till att förfina. nuvarande strategierna för ASCVD-riskbedömning, och det är det beräknas vara förhöjd i cirka 20% av världens befolkning. Forskning på Lp (a) antyder att det har ett mervärde i förebyggande medicin, och det är dags för kardiologer och kardiovaskulära teammedlemmar att överväga att använda det rutinmässigt i sin praktik. Baserat på de ökande bevisen publicerade Wilson et al nyligen en riktlinje om den kliniska användningen av Lp (a) från National Lipid Association, och här sammanfattar vi viktiga delar av deras arbete.
Vad är Lipoprotein (a )?
Lipoprotein (a) är en lågdensitetslipoprotein (LDL) -partikel med ett tillsatt apolipoprotein (a) (apo) fäst till apoplipoprotein (b) (apo) -komponenten i LDL-partikeln via en disulfidbro. Strukturen för Lp (a) är mycket heterogen sekundär till många olika apo (a) isoformer inom befolkningen. Etiologiskt kan det ha gett en överlevnadsfördel genom att hjälpa sårläkning och minska blödning, särskilt vid förlossning. En individuell Lp (a) -nivå är 80-90% genetiskt bestämd i ett autosomalt kodominant arvsmönster med fullt uttryck vid 1-2 års ålder och vuxenliknande nivåer uppnådda vid ungefär 5 års ålder. Utanför akuta inflammatoriska tillstånd , Lp (a) -nivån förblir stabil under en individs livstid oavsett livsstil.
Tidiga data tyder på en koppling mellan Lp (a) -nivå och både ASCVD och valvular aortastenos (VAS), men den exakta patofysiologiska mekanismen är inte helt klar. En aktuell teori inkluderar ett tvåkantigt bidrag från Lp (a) -molekylen. Apo (a) har homologi med plasminogen och har visats in vitro att hämma fibrinolys. Därför kan det hypotetiskt främja trombos vid sårbara arteriella plack eller turbulent flöde i stenos som orsakar obstruktion eller främjar bildning av emboli i VAS. Den LDL-liknande delen kan främja intim kolesterolavsättning men kolesterolhalten i till och med mycket höga nivåer av Lp (a) ligger under traditionella LDL-gränsvärden och bidrar sannolikt mindre. Nyare bevis tyder på att oxiderade fosfolipider samlokaliseras med Lp (a) -molekyler och tillsammans kan främja endotel dysfunktion, inflammation och förkalkning i kärlsystemet.
Högkvalitativa bevis stöder en koppling mellan Lp (a) -nivåer och en mängd olika kardiovaskulära resultat. En metaanalys visade en ökad risk för CHD och MI med koncentrationer > 30 mg / dL (62 nmol / L) medan INTERHEART-studien visade Lp (a) > 50 mg / dL var associerad med ökad risk för MI (ELLER 1,48; 95% KI 1,32-1,67; P < 0,001). Samma metaanalys visade ökad risk för stroke vid Lp (a) < 50 mg / dL och en annan visade en 2x högre risk för ischemisk stroke med mindre apo (a) isoformer. Tabell 1 visar risken för förhöjd Lp (a) på en mängd olika kardiovaskulära tillstånd baserat på stora prospektiva, befolkningsbaserade studier och att dessa föreningar också sågs i randomiseringsstudier i mendel. Slutligen fann genomgående associeringsstudier med fokus på genetisk variation och risk för sjukdom att höga Lp (a) -koncentrationer ger den högsta risken för ASCVD och VAS oberoende av andra kända orsaker och riskfaktorer.
Tabell 1: Effekten av förhöjda Lp (a) -nivåer på olika kliniska resultat baserat på stora prospektiva, befolkningsbaserade studier och om dessa slutsatser stöddes av stora mendeliska randomiseringsstudier.

Tabell 1

Tabell 1: Effekt av förhöjd Lp (a ) nivåer på olika kliniska resultat baserat på stora prospektiva, befolkningsbaserade studier och huruvida dessa slutsatser stöddes av stora mendeliska randomiseringsstudier.
Mätning och målnivåer för Lp (a)
Ett av de största hindren för den kliniska användningen av Lp (a) är att dess mätning och målnivåer inte har standardiserats. Flera tillgängliga analyser rapporterar resultat i massa (mg / dL) istället för koncentration (nmol / L), varav den senare föredras. Till skillnad från andra lipider och lipoproteiner är direkt omvandling mellan dessa två enheter inte möjlig på grund av det variabla antalet upprepade enheter i olika apo (a) isoformer, vilket leder till över- eller underskattning beroende på partikelstorleken. Oavsett analys eller enheter som används varierar Lp (a) -nivåerna mellan etniska grupper och sjukdomstillstånd, liksom om mätningarna var från färska eller frysta prover, vilket har gjort publicerade målnivåer inkonsekventa. Lyckligtvis kan alla dessa övervinnas genom standardisering av analysen och genererade mätningar. Riktlinjen rekommenderar att Lp (a) -nivåer rapporteras som koncentration (nmol / L) med hjälp av en analys kalibrerad mot WHO / International Federation of Clinical Chemistry and Laboratory Medicine sekundärreferenshandbok.
Baserat på tillgängliga studier, riktlinje rekommenderar en universell skärpunkt på ≥100 nmol / L (ungefär ≥50 mg / dL), vilket ungefär den 80: e percentilen i de kaukasiska amerikanska befolkningarna. Användningen av denna skärpunkt förblir emellertid ett diskussionsämne bland många experter i lipidsamhället och detta beror sannolikt på bristen på standardisering och epidemiologiska skillnader. Denna kontrovers representeras av riktlinjerna för American Heart Association (ACC) / American Heart Association (AHA) 2018, vilket tyder på att hög risk är ≥125 nmol / L (eller ≥50 mg / dL). Avskärningen kan förändras när ytterligare studier är slutförda, med tanke på att avskärningen kan variera beroende på risk, etnicitet och comorbiditeter.
Vilka patienter borde ha mätt Lp (a)?
Om man antar tillgång till en WHO-standardiserad analys kan utvalda patienter ha nytta av Lp (a) -test efter en gemensam beslutsdiskussion är klart. Baserat på denna riktlinje kan mätning av Lp (a) vara rimligt hos patienter med en personlig historia av eller förstegrads släkting med för tidig ASCVD (särskilt om annars anses låg risk) och i svår hyperkolesterolemi (LDL-C ≥190 mg / dL). Testning hos dessa patienter kan utlösa eskalering av behandlingen, såsom beskrivs nedan. Ytterligare indikationer där testning kan vara rimliga listas i tabell 2, särskilt patienter med LDL-C-respons på statiner är mindre än förväntat, eller hos patienter med gränsrisk (5% till ≤ 7,5% 10-årig ASCVD-risk) som är särskilt intresserade av att minska sin ASCVD-risk.
Tabell 2: Populationer där Lp (a) -testning kan vara rimlig baserat på aktuella bevis.
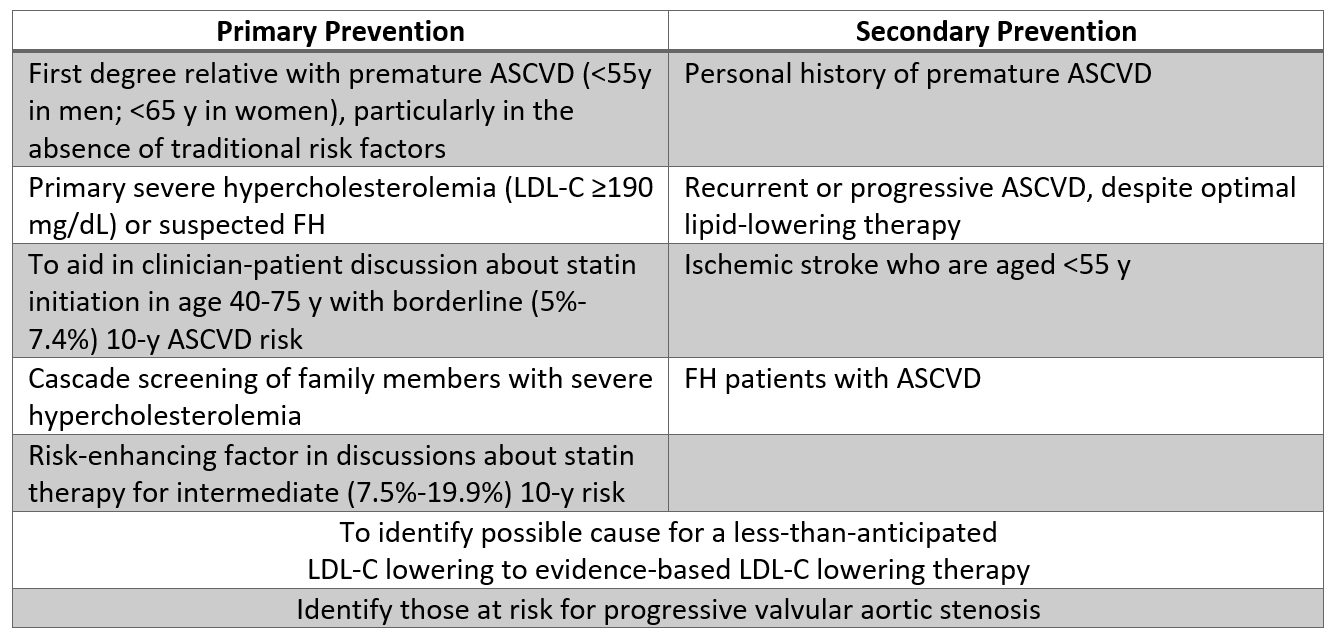
Tabell 2

Tabell 2: Populationer där Lp (a) -testning kan vara rimlig baserat på aktuella bevis.
Studier som en JUPITER (Motivering för användning av statiner i förebyggande syfte: En interventionsstudie som utvärderar Rosuvastatin) delanalys visar Lp (a) är en stark förutsägelse för risk när den förblir förhöjd hos patienter som redan har statin. Ingen tillgänglig data stöder dock att behandling av isolerat, förhöjt Lp (a) leder till bättre kliniska resultat. Om och när riktad Lp (a) -behandling blir tillgänglig kan det vara rimligt att starta universell screening i ung ålder för att avgöra om tidigare förebyggande åtgärder anges.
Intressant kan det finnas en mer akut effekt som nuvarande bevis visar en koppling mellan förhöjd Lp (a) och ischemisk stroke hos ungdomar. Därför kan det vara rimligt att mäta Lp (a) hos ungdomar med genetiskt bekräftad eller kliniskt misstänkt familjär hyperkolesterolemi (FH), familjehistoria av första gradens släkting med för tidig ASCVD, eller ischemisk stroke eller en förälder / syskon som befunnits ha förhöjt Lp (a). Men med tanke på att Lp (a) -nivåer förblir stabila under hela sitt liv utanför akut inflammation, finns det inte mycket rollmätning av Lp (a) -nivåer för närvarande.
Hur behandlar du Förhöjt Lp (a)?
Trots de observerade föreningarna mellan förhöjd Lp (a) och ASCVD, har det ännu inte funnits en randomiserad kontrollerad studie för att se om riktad sänkning av Lp (a) förbättrar kliniska resultat. har Lp (a) -sänkande effekten av för närvarande tillgängliga terapier undersökts.
Av de nuvarande tillgängliga förebyggande terapierna är endast ett begränsat antal effektivt för att minska Lp (a).I den avgörande prövningen av evolocumab (FOURIER – Ytterligare kardiovaskulära resultat undersökta med PCSK9-hämning hos patienter med förhöjd risk) minskade en PCSK9-hämmare, Lp (a) med 27% och den observerade minskningen av större negativa kardiovaskulära händelser (MACE) var störst för dem med de högsta baslinjenivåerna Lp (a). På samma sätt hade alirocumab (i ODYSSEY-RESULTAT – Utvärdering av kardiovaskulära resultat efter och akut koronarsyndrom under behandling med Alirocumab) ökad MACE-minskning hos individer med högre baslinje-Lp (a) -nivåer. Även om dessa resultat är uppmuntrande är effekterna av PCSK9-hämmare på Lp (a) ganska blygsamma, och ytterligare analys behövs innan PCSK9-hämmare kan rekommenderas som Lp (a) -riktad terapi.
Aferes kan övervägas för utvalda patienter. Det är mycket effektivt för att sänka nivåerna Lp (a) men ett kostsamt och besvärligt förfarande som kan vara svårt att få försäkringsskydd för. Det är reserverat för endast de mest eldfasta patienterna och bör bedrivas efter att ha kontrollerat kända riskfaktorer optimalt med beprövad behandling. I Tyskland tycktes aferes ge en 70% minskning av MACE hos patienter med återkommande ASCVD-händelser med förhöjd Lp (a) oavsett LDL-C-nivåer.
Det är viktigt att ett antal vanliga förebyggande strategier är ineffektiva. Framför allt minskar livsstilsförändringar, inklusive kost och motion, inte Lp (a). Tidiga data om statiner visade blandade resultat med vissa studier som tyder på att de till och med kan leda till ökningar av Lp (a). Men mer samtida studier visar att statinbehandling i sig påverkar Lp (a) -nivåerna; men viktigt är att de som fortsätter att ha höga Lp (a) -nivåer på ett statin har ökad ASCVD-risk även om LDL-C förbättras. Hormonersättningsterapi minskar Lp (a), men dess användning begränsas av överflödig ökning av biverkningar. Niacin minskar Lp (a) 23% men förbättrade inte ASCVD-resultaten baserat på AIM HIGH (Niacin Plus Statin för att förhindra vaskulära händelser) och HPS2 THRIVE (Behandling av HDL för att minska förekomsten av vaskulära händelser). Även om det tolereras av vissa, är niacin också förknippat med betydande biverkningar. Dessutom är dess effekt begränsad hos dem som kan dra nytta av mest (liten isoformstorlek och högsta Lp-nivå vid baslinjen).
Baserat på tillgängliga data rekommenderar författarna att man startar en måttlig till hög intensitetsstatinbehandling hos vuxna i åldrarna 40-75 år med en 10-årig ASCVD-risk på 7,5% till ≤20% med en Lp (a) ≥100 nmol / L. Som redan vanligt görs bör högriskpatienter med LDL-C ≥70 mg / dL (icke-HDL-C ≥100 mg / dL) och en Lp (a) ≥100 nmol / L på maximalt tolererat statin övervägas för mer intensiva terapier (ezetimib och PCSK9-hämmare) för att sänka LDL-C.
För närvarande studeras nya terapier som selektivt riktar sig mot Lp (a). En fas 2-studie av AKCEA apo (a) -LRx, en apo (a) antisense-oligonukleotid, reducerade Lp (a) upp till 80%. En fas 3-studie planeras. Dessutom har en oxPL-antikropp som binder och inaktiverar den pro-osteogena aktiviteten hos Lp (a) lovande in vitro-data. Dessa terapier, även om de är lovande, kräver ytterligare forskning innan de blir vanliga terapier.
Slutsats
Lipoprotein (a) representerar en spännande ny biomarkör inom lipidologi och förebyggande kardiologi. Förhöjd Lp (a) är kausalt inblandad i ASCVD, och testning hos specifika patienter kan hjälpa till att skräddarsy lämplig intensitet av förebyggande åtgärder. Men på grund av bristen på standardisering och heterogenitet hos tillgängliga data är optimala avstängningar fortfarande en källa till intensiv debatt. Det nuvarande fokuset för klinisk vård är på traditionell riskfaktorkontroll hos patienter med hög Lp (a) eftersom riktade behandlingsalternativ är begränsade. Nya Lp (a) -inriktade terapier undersöks aktivt, och om de lyckas kan de bli en viktig del av primär och sekundär förebyggande.
Kliniska ämnen: Akuta koronarsyndrom, Diabetes och kardiometabolisk sjukdom, Dyslipidemi, Förebyggande, Valvulär hjärtsjukdom , ACS- och hjärtbiomarkörer, avancerad lipidtestning, homozygot familjär hyperkolesterolemi, lipidmetabolism, nonstatiner, nya medel, primär hyperlipidemi, statiner, diet
Nyckelord: Dyslipidemier, akut koronarsyndrom, American Heart Association, antikroppar, monoklonal , Aortaklaffstenos, Apolipoproteiner A, Apolipoproteiner B, Borttagning av blodkomponenter, hjärniskemi, biologiska markörer, kardiovaskulära sjukdomar, kolesterol, kemi, klinisk, förträngning, patologisk, komorbiditet, diet, disulfider, beslutsfattande, etniska grupper, fibrinolys, gen Bred associeringsstudie, genetisk variation, hormonersättningsterapi, hydroximetylglutaryl-CoA-reduktashämmare, hyperkolesterolemi, hyperlipoproteinemi typ II, inflammation, arvsmönster, livsstil, försäkringsskydd ålder, Lipoprotein (a), Lipoproteiner, LDL, Niacin, Oligonukleotider, Antisense, Partikelstorlek, Fosfolipider, Plasminogen, Prospektiva studier, Proteinisformer, Slumpmässig allokering, Riskfaktorer, Riskbedömning, Sekundär förebyggande, Stroke, Trombos, Världshälsoorganisationen, Subtilisins
< Tillbaka till listor