Vannets overflatespenning er omtrent 72 mN / m ved romtemperatur, noe som er en av de høyeste overflatespenningene for væske. Det er bare en væske med høyere overflatespenning, og det er kvikksølv, som er et flytende metall med overflatespenningen på nesten 500 mN / m. Hvorfor overflatespenning av kvikksølv er så høy, vil også være tydelig etter å ha lest dette korte blogginnlegget.
Den høye overflatespenningen til vann er forårsaket av sterke molekylære interaksjoner
Overflatespenningen oppstår pga. til sammenhengende interaksjoner mellom molekylene i væsken. På hovedparten av væsken har molekylene nabomolekyler på hver side. Molekyler trekker hverandre likt i alle retninger og forårsaker en nettokraft på null. Imidlertid, ved grensesnittet, har de flytende molekylene bare halvparten av de nærliggende flytende molekylene sammenlignet med hoveddelen av væsken. Dette gjør at molekylet assosieres sterkere med molekylene på sidene og forårsaker en netto innadgående kraft mot væsken. Denne kraften motstår brudd på overflaten og kalles overflatespenning.
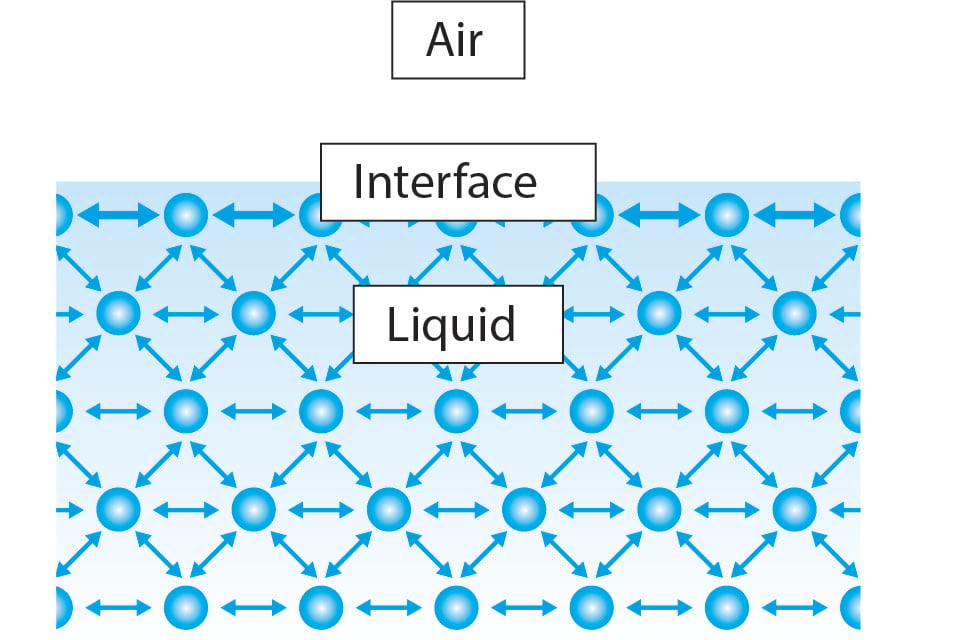
Med denne forklaringen i tankene er det da klart at alle væskene vil ha den samme egenskapen, men hvorfor overflatespenningen til vann er mye høyere enn for eksempel etanol.
For å forstå dette må vi tenke på båndene mellom molekylene. Som forklart forårsaker den sammenhengende kraften mellom molekylene overflatespenning. Jo sterkere den sammenhengende kraften, jo sterkere blir overflatespenningen. Vannmolekylet har to hydrogenatomer bundet til et oksygenatom gjennom kovalent binding. På grunn av den høye elektronegativiteten til oksygen, vil den ha en stor del av den negative ladningen på siden, mens hydrogen vil være mer positivt ladet. Dette forårsaker en elektrostatisk tiltrekning mellom hydrogenatomet i ett molekyl og oksygenatomet i et annet. Dannede bindinger kalles hydrogenbindinger som fører til sterke sammenhengende krefter mellom vannmolekylene og høy overflatespenning av vann.
Som nevnt i begynnelsen av bloggen, forklarer dette også hvorfor kvikksølv har så høy overflatespenning. Siden kvikksølv er et metall, er bindingene mellom molekylene metallbindinger som er mye sterkere enn hydrogenbindinger som fører til svært høye sammenhengende krefter og høy overflatespenning.
For å lære mer om viktigheten av overflatespenning gjennom lenken nedenfor
