Editors Note: Commentary based on Wilson DP, Jacobson TA, Jones PH, et al. Use of Lipoprotein (a) i klinisk praksis: en biomarkør hvis tid er kommet. En vitenskapelig uttalelse fra National Lipid Association. J Clin Lipidol 2019; 13: 374-92.
Innledning
Den tradisjonelle lipidprofilen har tjent som en bærebjelke i risikovurdering av aterosklerotisk kardiovaskulær sykdom (ASCVD) i flere tiår. Dette verktøyet ble enda viktigere ettersom målrettede terapier, som statiner og nylig ezetimib og proprotein convertase subtilisin / kexin type 9 (PCSK9) -hemmere, ble tilgjengelig. Selv med disse fremskrittene innen lipidbehandling, og mer bredt når det gjelder å målrette tradisjonelle kardiovaskulære risikofaktorer, peker pågående risiko hos mange pasienter på et behov for å undersøke andre bidragsytere som mulige terapeutiske mål. gjeldende strategier for ASCVD risikovurdering, og det er det anslått å være forhøyet i omtrent 20% av verdens befolkning. Forskning på Lp (a) antyder at den har merverdi i forebyggende medisin, og det er på tide for kardiologer og kardiovaskulære teammedlemmer å vurdere å bruke det rutinemessig i sin praksis. Basert på de økende bevisene, publiserte Wilson et al nylig en retningslinje for klinisk bruk av Lp (a) fra National Lipid Association, og her oppsummerer vi nøkkelelementene i deres arbeid.
Hva er Lipoprotein (a )?
Lipoprotein (a) er en lipoprotein (LDL) -partikkel med lav tetthet med et tilsatt apolipoprotein (a) (apo) festet til apoplipoprotein (b) (apo) komponent av LDL-partikkelen via en disulfidbro. Strukturen til Lp (a) er svært heterogen sekundær til mange forskjellige apo (a) isoformer i befolkningen. Etiologisk kan det ha gitt en overlevelsesfordel ved å hjelpe sårheling og redusere blødning, spesielt i fødsel. Et individuelt Lp (a) -nivå er 80-90% genetisk bestemt i et autosomalt kodominant arvemønster med fullt uttrykk ved 1-2 års alder og voksenlignende nivåer oppnådd med omtrent 5 års alder. Utenfor akutte betennelsestilstander , forblir Lp (a) -nivået stabilt gjennom individets levetid uavhengig av livsstil.
Tidlige data antyder en sammenheng mellom Lp (a) -nivå og både ASCVD og valvular aortastenose (VAS), men den eksakte patofysiologiske mekanismen er ikke helt klar. En aktuell teori inkluderer et todelt bidrag fra Lp (a) -molekylet. Apo (a) har homologi med plasminogen og har vist seg in vitro å hemme fibrinolyse. Derfor kan det hypotetisk fremme trombose ved sårbare arterielle plakk eller turbulent strømning i stenose og forårsake obstruksjon eller fremme dannelse av emboli i VAS. Den LDL-lignende delen kan fremme intimal kolesterolavsetning, men kolesterolinnholdet i til og med svært høye nivåer av Lp (a) er under tradisjonelle LDL-avskjæringer og bidrar sannsynligvis mindre. Nyere bevis antyder at oksyderte fosfolipider samlokaliserer seg med Lp (a) -molekyler og sammen kan fremme endotel dysfunksjon, betennelse og forkalkning i vaskulaturen.
Bevis av høy kvalitet støtter en sammenheng mellom Lp (a) nivåer og en rekke kardiovaskulære relaterte resultater. En metaanalyse viste en økt risiko for CHD og MI med konsentrasjoner > 30 mg / dL (62 nmol / L) mens INTERHEART-studien viste Lp (a) > 50 mg / dL var assosiert med økt risiko for MI (ELLER 1,48; 95% KI 1,32-1,67; P < 0,001). Den samme metaanalysen viste økt risiko for hjerneslag ved Lp (a) < 50 mg / dL og en annen viste en 2x høyere risiko for iskemisk hjerneslag med mindre apo (a) isoformer. Tabell 1 viser risikoen for forhøyet Lp (a) på en rekke kardiovaskulære tilstander basert på store prospektive, populasjonsbaserte studier, og at disse assosiasjonene også ble sett i Mendel-randomiseringsstudier. Til slutt viste genomdekkende assosiasjonsstudier med fokus på genetisk variasjon og risiko for sykdom at høye Lp (a) konsentrasjoner gir høyest risiko for ASCVD og VAS uavhengig av andre kjente årsaker og risikofaktorer.
Tabell 1: Effekt av forhøyede Lp (a) nivåer på forskjellige kliniske utfall basert på store prospektive, populasjonsbaserte studier og om disse konklusjonene ble støttet av store randomiserte Mendelian-studier.

Tabell 1

Tabell 1: Effekt av forhøyet Lp (a ) nivåer på ulike kliniske utfall basert på store prospektive, populasjonsbaserte studier og om disse konklusjonene ble støttet av store mandeliske randomiseringsstudier.
Måling og målnivåer av Lp (a)
En av de viktigste hindringene for den kliniske bruken av Lp (a) er at måling og målnivå ikke har blitt standardisert. Flere tilgjengelige analyser rapporterer resultater i masse (mg / dL) i stedet for konsentrasjon (nmol / L), hvor sistnevnte er foretrukket. I motsetning til andre lipider og lipoproteiner er direkte konvertering mellom disse to enhetene ikke mulig på grunn av det variable antallet gjentatte enheter i forskjellige apo (a) isoformer, noe som fører til over- eller undervurdering avhengig av partikkelstørrelse. Uavhengig av analysen eller enhetene som brukes, varierer Lp (a) nivåene mellom etniske grupper og sykdomstilstander, samt om målingene var fra ferske eller frosne prøver, noe som har gjort publiserte målnivåer inkonsekvente. Heldigvis kan alle disse overvinnes ved standardisering av analysen og genererte målinger. Retningslinjen anbefaler å rapportere Lp (a) nivåer som konsentrasjon (nmol / L) ved hjelp av en analyse kalibrert mot WHO / International Federation of Clinical Chemistry and Laboratory Medicine sekundær referansehåndbok.
Basert på tilgjengelige studier, er retningslinje anbefaler et universelt kuttpunkt på ≥100 nmol / L (omtrent ≥50 mg / dL), som tilnærmer 80. persentilen i de kaukasiske amerikanske befolkningene. Imidlertid er bruken av dette kuttpunktet fortsatt et tema for debatt blant mange eksperter i lipidsamfunnet, og dette stammer sannsynligvis fra mangel på standardisering og epidemiologiske forskjeller. Denne kontroversen er representert av 2018 American Heart Association (ACC) / American Heart Association (AHA) kolesterolretningslinjer, som antyder at høy risiko er ≥125 nmol / L (eller ≥50 mg / dL). Avskjæringen kan endres etter hvert som flere studier er fullført, og erkjenner at avskjæringen kan variere basert på risiko, etnisitet og komorbiditeter.
Hvilke pasienter burde ha målt Lp (a)?
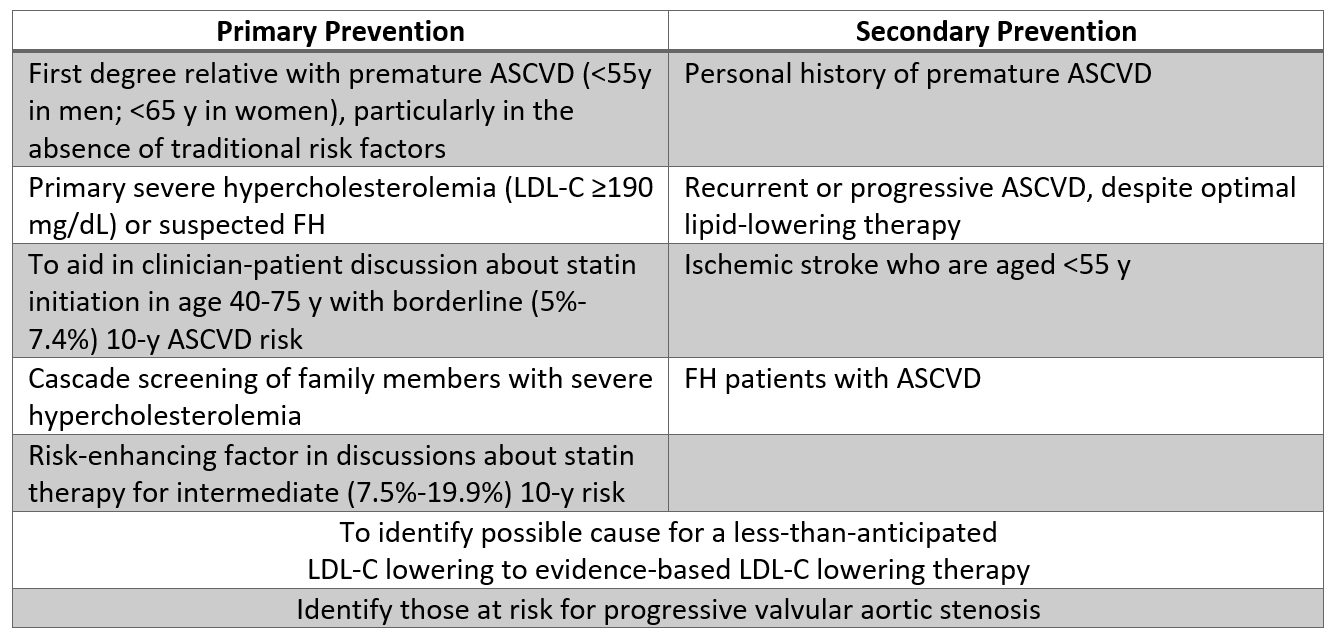
Forutsatt tilgang til en WHO-standardisert analyse, kan utvalgte pasienter ha nytte av Lp (a) -testing etter en delt beslutningsdiskusjon det er ferdig. Basert på denne retningslinjen kan måling av Lp (a) være rimelig hos pasienter med en personlig historie med eller førstegrads slektning med for tidlig ASCVD (spesielt hvis det ellers anses som lavrisiko), og i alvorlig hyperkolesterolemi (LDL-C ≥190 mg / dL). Testing hos disse pasientene kan utløse opptrapping av behandlingen, som beskrevet nedenfor. Ytterligere indikasjoner der testing kan være rimelig er oppført i tabell 2, spesielt inkludert pasienter der LDL-C-responsen på statiner er mindre enn forventet, eller hos pasienter med grenserisiko (5% til ≤ 7,5% 10-års ASCVD-risiko) som er spesielt interessert i å redusere ASCVD-risikoen.
Tabell 2: Populasjoner der Lp (a) -testing kan være rimelig basert på gjeldende bevis.
Tabell 2

Tabell 2: Populasjoner der Lp (a) -testing kan være rimelig basert på gjeldende bevis.
Undersøkelser som en JUPITER (begrunnelse for bruk av statiner i forebygging: En intervensjonsforsøk som evaluerer Rosuvastatin) delanalyse viser Lp (a) er en sterk prediktor for risiko når den forblir forhøyet hos pasienter som allerede har statin. Imidlertid støtter ingen tilgjengelige data at behandling av isolert, forhøyet Lp (a) fører til bedre kliniske resultater. Hvis og når målrettet behandling med Lp (a) blir tilgjengelig, kan det være rimelig å starte universell screening i ung alder for å avgjøre om tidligere forebyggende tiltak er indikert.
Interessant kan det være en mer akutt effekt som nåværende bevis viser en sammenheng mellom forhøyet Lp (a) og iskemisk hjerneslag hos ungdom. Derfor kan det være rimelig å måle Lp (a) i ungdom med genetisk bekreftet eller klinisk mistenkt familiær hyperkolesterolemi (FH), familiehistorie av første graders slektning med for tidlig ASCVD, eller iskemisk hjerneslag eller en foreldre / søsken som har funnet å ha forhøyet Lp (en). Men gitt at Lp (a) nivåer holder seg stabile gjennom hele livet utenfor akutt betennelse, er det ikke mye rolle seriemåling av Lp (a) nivåer på det nåværende tidspunkt.
Hvordan behandler du Forhøyet Lp (a)?
Til tross for de observerte assosiasjonene mellom forhøyet Lp (a) og ASCVD, har det ennå ikke vært en randomisert kontrollert studie for å se om målrettet senking av Lp (a) forbedrer kliniske resultater. , den Lp (a) -lowerende effekten av for tiden tilgjengelige terapier er undersøkt.
Av de nåværende tilgjengelige forebyggende terapiene er bare et begrenset antall effektive for å redusere Lp (a).I den sentrale studien av evolocumab (FOURIER – Ytterligere kardiovaskulære utfall undersøkt med PCSK9-hemming hos pasienter med forhøyet risiko), ble en PCSK9-hemmer, Lp (a) redusert med 27%, og den observerte reduksjonen i større ugunstige kardiovaskulære hendelser (MACE) var størst for de med de høyeste baseline Lp (a) nivåene. Tilsvarende hadde alirocumab (i ODYSSEY RESULTATER – Evaluering av kardiovaskulære utfall etter og akutt koronarsyndrom under behandling med Alirocumab) økt MACE reduksjon hos individer med høyere baseline Lp (a) nivåer. Selv om disse resultatene er oppmuntrende, er virkningen av PCSK9-hemmere på Lp (a) ganske beskjeden, og det er behov for ytterligere analyse før PCSK9-hemmere kan anbefales som Lp (a) -målrettet behandling.
Aferese kan vurderes for utvalgte pasienter. Det er svært effektivt for å senke Lp (a) nivåer, men en kostbar og tungvint prosedyre som kan være vanskelig å få forsikringsdekning for. Det er reservert for bare de mest ildfaste pasientene og bør forfølges etter optimal kontroll av kjente risikofaktorer med velprøvd behandling. I Tyskland så det ut til at averes ga en 70% reduksjon i MACE hos pasienter med tilbakevendende ASCVD-hendelser med forhøyet Lp (a) uavhengig av LDL-C-nivåer.
Det er viktig at en rekke ofte brukte forebyggende strategier er ineffektive. Spesielt reduserer livsstilsendringer, inkludert kosthold og trening, ikke Lp (a). Tidlige data om statiner viste blandede resultater med noen studier som antydet at de til og med kan føre til økning i Lp (a). Imidlertid viser mer moderne studier at statinbehandling i seg selv påvirker Lp (a) nivåer; men viktigere, de som fortsetter å ha høye Lp (a) nivåer på et statin har økt ASCVD risiko selv om LDL-C forbedres. Hormonerstatningsterapi reduserer Lp (a), men bruken av den er begrenset av overflødig økning i bivirkninger. Niacin reduserer Lp (a) 23%, men forbedret ikke ASCVD-resultatene basert på AIM HIGH (Niacin Plus Statin for å forhindre vaskulære hendelser) og HPS2 THRIVE (Behandling av HDL for å redusere forekomsten av vaskulære hendelser) studier. Selv om det tolereres av noen, er niacin også forbundet med betydelige bivirkninger. Videre er dens effekt begrenset hos de som kan ha størst nytte (liten isoformstørrelse og høyeste baseline Lp-nivå).
Basert på tilgjengelige data, anbefaler forfatterne å starte en moderat til høy intensitetsstatinbehandling hos voksne i alderen 40-75 år med en 10-årig ASCVD-risiko på 7,5% til ≤20% med en Lp (a) ≥100 nmol / L. Som det allerede er gjort, bør høyrisikopasienter med LDL-C ≥70 mg / dL (ikke-HDL-C ≥100 mg / dL) og en Lp (a) ≥100 nmol / L på maksimalt tolerert statin vurderes for mer intensive terapier (ezetimib og PCSK9-hemmere) for å senke LDL-C.
For tiden studeres nye terapier som selektivt retter seg mot Lp (a). En fase 2-studie av AKCEA apo (a) -LRx, en apo (a) antisense-oligonukleotid, reduserte Lp (a) opp til 80%. En fase 3-studie planlegges. I tillegg har et oxPL-antistoff som binder og inaktiverer den pro-osteogene aktiviteten til Lp (a) lovende in vitro-data. Selv om disse behandlingene er lovende, krever det ytterligere forskning før de blir vanlige terapier.
Konklusjon
Lipoprotein (a) representerer en spennende ny biomarkør innen lipidologi og forebyggende kardiologi. Forhøyet Lp (a) er kausalt implisert i ASCVD, og testing hos spesifikke pasienter kan bidra til å skreddersy passende intensitet av forebyggende tiltak. Imidlertid, på grunn av mangel på standardisering og heterogenitet av tilgjengelige data, forblir optimale avskjæringer en kilde til intens debatt. Det nåværende fokuset for klinisk behandling er på tradisjonell risikofaktorkontroll hos pasienter med høy Lp (a), da målrettede behandlingsmuligheter er begrensede. Roman Lp (a) -målrettede terapier blir aktivt undersøkt, og hvis de lykkes, kan de bli en viktig komponent i primær og sekundær forebygging.
Kliniske temaer: Akutte koronarsyndrom, Diabetes og kardiometabolisk sykdom, Dyslipidemi, Forebygging, Valvulær hjertesykdom , ACS og kardiale biomarkører, avansert lipidprøving, homozygot familiær hyperkolesterolemi, lipidmetabolisme, ikke-statiner, nye midler, primær hyperlipidemi, statiner, diett , Aorta Valve Stenosis, Apolipoproteins A, Apolipoproteins B, Blood Component Removal, Brain Ischemia, Biological Markers, Cardiovascular Diseases, Cholesterol, Chemistry, Clinical, Constriction, Pathologic, Comorbidity, Diet, Disulfides, Decision Making, Ethnic Groups, Fibrinolysis, Genome Bred foreningsstudie, genetisk variasjon, hormonerstatningsterapi, hydroksymetylglutaryl-CoA-reduktasehemmere, hyperkolesterolemi, hyperlipoproteinemia type II, betennelse, arvsmønstre, livsstil, forsikringsdekning alder, Lipoprotein (a), Lipoproteiner, LDL, Niacin, Oligonukleotider, Antisense, Partikkelstørrelse, Fosfolipider, Plasminogen, Prospective Studies, Protein Isoforms, Random Allocation, Risk Factors, Risk Assessment, Secondary Prevention, Stroke, Thrombosis, World Health Organization, Subtilisins
< Tilbake til oppføringer