Nota del editor: Comentario basado en Wilson DP, Jacobson TA, Jones PH, et al. Uso de lipoproteína (a) en la práctica clínica: un biomarcador cuyo momento ha llegado. Declaración científica de la Asociación Nacional de Lípidos. J Clin Lipidol 2019; 13: 374-92.
Introducción
El perfil lipídico tradicional ha servido como un pilar de la evaluación del riesgo de enfermedad cardiovascular aterosclerótica (ASCVD) durante décadas. Esta herramienta se volvió aún más importante a medida que las terapias dirigidas, como las estatinas y, más recientemente, ezetimiba y los inhibidores de la subtilisina / kexina tipo 9 de proproteína convertasa (PCSK9) se pusieron a disposición. Incluso con estos avances en el manejo de lípidos, y más ampliamente en la focalización de factores de riesgo cardiovascular tradicionales, el riesgo continuo en muchos pacientes apunta a la necesidad de investigar otros contribuyentes como posibles dianas terapéuticas. La lipoproteína (a) (Lp) es un biomarcador prometedor para ayudar a refinar estrategias actuales de evaluación de riesgos ASCVD, y es se estima que es elevado en aproximadamente el 20% de la población mundial. La investigación sobre la Lp (a) sugiere que tiene un valor agregado en la medicina preventiva, y es hora de que los cardiólogos y los miembros del equipo cardiovascular consideren su uso rutinario en su práctica. Con base en la creciente evidencia, Wilson et al publicaron recientemente una guía sobre el uso clínico de Lp (a) de la National Lipid Association, y aquí resumimos los elementos clave de su trabajo.
¿Qué es la lipoproteína (a )?
La lipoproteína (a) es una partícula de lipoproteína de baja densidad (LDL) con una apolipoproteína (a) (apo) añadida unida al componente apoplipoproteína (b) (apo) de la partícula LDL a través de un puente disulfuro. La estructura de Lp (a) es muy heterogénea secundaria a muchas isoformas de apo (a) diferentes dentro de la población. Etiológicamente, puede haber proporcionado una ventaja de supervivencia al ayudar en la curación de heridas y reducir el sangrado, particularmente en el parto. El nivel de Lp (a) de un individuo está determinado genéticamente en un 80-90% en un patrón de herencia codominante autosómico con expresión completa a los 1-2 años de edad y niveles similares a los de los adultos alcanzados aproximadamente a los 5 años de edad. Fuera de los estados inflamatorios agudos , el nivel de Lp (a) permanece estable a lo largo de la vida de un individuo independientemente de su estilo de vida.
Los primeros datos sugieren un vínculo entre el nivel de Lp (a) y la ASCVD y la estenosis aórtica valvular (EVA), pero el mecanismo fisiopatológico exacto no está del todo claro. Una teoría actual incluye una contribución doble de la molécula Lp (a). Apo (a) tiene homología con el plasminógeno y se ha demostrado in vitro que inhibe la fibrinólisis. Por lo tanto, hipotéticamente podría promover la trombosis en las placas arteriales vulnerables o el flujo turbulento dentro de la estenosis que causa obstrucción o promueve la formación de émbolos en la EAV. La porción similar a LDL puede promover la deposición de colesterol en la íntima, pero el contenido de colesterol incluso en niveles muy altos de Lp (a) está por debajo de los límites de LDL tradicionales y probablemente contribuya menos. La evidencia más reciente sugiere que los fosfolípidos oxidados co-localizan con las moléculas de Lp (a) y juntos pueden promover disfunción endotelial, inflamación y calcificación en la vasculatura.
La evidencia de alta calidad respalda un vínculo entre los niveles de Lp (a) y una variedad de resultados relacionados con el sistema cardiovascular. Un metanálisis mostró un mayor riesgo de cardiopatía coronaria e infarto de miocardio con concentraciones > 30 mg / dL (62 nmol / L), mientras que el ensayo INTERHEART mostró Lp (a) > 50 mg / dL se asoció con un mayor riesgo de infarto de miocardio (OR 1,48; IC del 95%: 1,32-1,67; P < 0,001). El mismo metanálisis mostró un mayor riesgo de accidente cerebrovascular en Lp (a) < 50 mg / dL y otro mostró un riesgo 2 veces mayor de accidente cerebrovascular isquémico con isoformas apo (a) más pequeñas. La Tabla 1 muestra el riesgo de Lp (a) elevado en una variedad de condiciones cardiovasculares basado en grandes estudios prospectivos basados en la población y que estas asociaciones también se observaron en estudios de aleatorización mendeliana. Finalmente, los estudios de asociación de todo el genoma que se centran en la variación genética y el riesgo de enfermedad encontraron que las concentraciones altas de Lp (a) confieren el mayor riesgo de ASCVD y VAS independientemente de otras causas y factores de riesgo conocidos.
Tabla 1: Impacto de los niveles elevados de Lp (a) en varios resultados clínicos basados en grandes estudios prospectivos basados en la población y si estas conclusiones fueron respaldadas por grandes estudios de aleatorización mendeliana.

Tabla 1

Tabla 1: Impacto de la Lp elevada (a ) niveles en varios resultados clínicos basados en grandes estudios prospectivos basados en la población y si estas conclusiones fueron respaldadas por grandes estudios de aleatorización mendeliana.
Medición y niveles objetivo de Lp (a)
Uno de los principales obstáculos para el uso clínico de Lp (a) es que su medición y niveles objetivo no se han estandarizado. Varios ensayos disponibles informan resultados en masa (mg / dL) en lugar de concentración (nmol / L), la última de las cuales se prefiere. A diferencia de otros lípidos y lipoproteínas, la conversión directa entre estas dos unidades no es posible debido al número variable de unidades repetidas en diferentes isoformas de apo (a), lo que conduce a una sobreestimación o subestimación según el tamaño de partícula. Independientemente del ensayo o las unidades utilizadas, los niveles de Lp (a) varían entre los grupos étnicos y los estados de enfermedad, así como si las mediciones fueron de muestras frescas o congeladas, lo que ha hecho que los niveles objetivo publicados sean inconsistentes. Afortunadamente, todos estos pueden superarse mediante la estandarización del ensayo y las mediciones generadas. La guía recomienda reportar los niveles de Lp (a) como concentración (nmol / L) usando un ensayo calibrado con el manual de referencia secundario de la OMS / Federación Internacional de Química Clínica y Medicina de Laboratorio.
Basado en los estudios disponibles, el La guía recomienda un punto de corte universal de ≥100 nmol / L (aproximadamente ≥50 mg / dL), que se aproxima al percentil 80 en las poblaciones caucásicas de EE. UU. Sin embargo, el uso de este punto de corte sigue siendo un tema de debate entre muchos expertos en la comunidad de lípidos y esto probablemente se deba a la falta de estandarización y diferencias epidemiológicas. Esta controversia está representada por las Pautas de colesterol de la American Heart Association (ACC) / American Heart Association (AHA) de 2018, que sugieren que el riesgo alto es ≥125 nmol / L (o ≥50 mg / dL). El límite puede cambiar a medida que se completen estudios adicionales, reconociendo que el límite puede variar según el riesgo, la etnia y las comorbilidades.
¿A qué pacientes se debe medir la Lp (a)?
Suponiendo que tengan acceso a un ensayo estandarizado por la OMS, algunos pacientes pueden beneficiarse de la prueba de Lp (a) después de una discusión compartida sobre la toma de decisiones esta completado. Con base en esta guía, la medición de Lp (a) puede ser razonable en pacientes con antecedentes personales o parientes de primer grado con ASCVD prematura (particularmente si se considera de bajo riesgo), y en hipercolesterolemia severa (LDL-C ≥ 190 mg / dL). Las pruebas en estos pacientes pueden desencadenar un aumento de la terapia, como se describe a continuación. Las indicaciones adicionales en las que las pruebas pueden ser razonables se enumeran en la Tabla 2, más notablemente incluidos los pacientes en los que la respuesta del C-LDL a las estatinas es menor de lo esperado, o en pacientes con riesgo límite (5% a ≤ 7.5% de riesgo de ASCVD a 10 años) están particularmente interesados en reducir su riesgo de ASCVD.
Tabla 2: Poblaciones en las que las pruebas de Lp (a) pueden ser razonables según la evidencia actual.
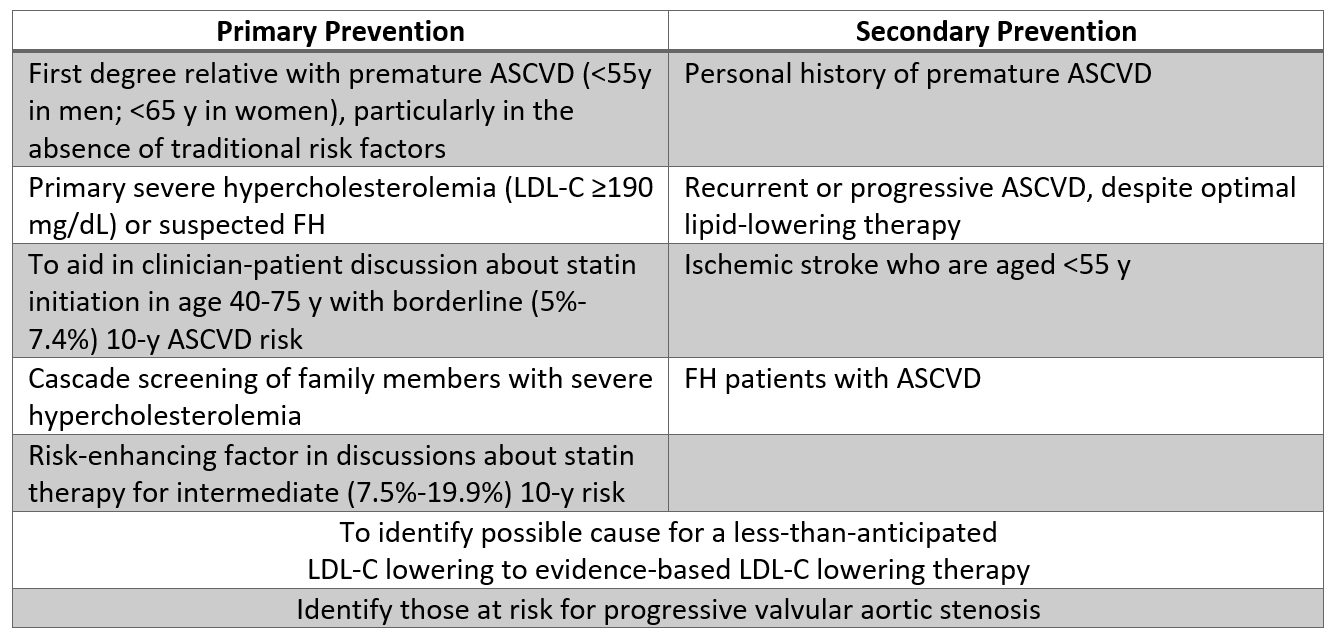
Tabla 2

Tabla 2: Poblaciones en las que las pruebas de Lp (a) pueden ser razonables según la evidencia actual.
Los estudios como un subanálisis de JUPITER (Justificación para el uso de estatinas en la prevención: un ensayo de intervención que evalúa la rosuvastatina) muestran un subanálisis de Lp (a) es un fuerte predictor de riesgo cuando permanece elevado en pacientes que ya están tomando una estatina. Sin embargo, no hay datos disponibles que apoyen que el tratamiento de Lp (a) elevado y aislado conduzca a mejores resultados clínicos. Si el tratamiento dirigido a Lp (a) está disponible, puede ser razonable comenzar la detección universal a una edad temprana para determinar si están indicadas medidas preventivas más tempranas.
Curiosamente, puede haber un efecto más agudo como La evidencia actual muestra un vínculo entre Lp (a) elevado y accidente cerebrovascular isquémico en la juventud. Por lo tanto, puede ser razonable medir la Lp (a) en jóvenes con hipercolesterolemia familiar (HF) confirmada genéticamente o sospechada clínicamente, antecedentes familiares de un pariente de primer grado con ASCVD prematuro o accidente cerebrovascular isquémico o un padre / hermano con Lp elevada. (a). Sin embargo, dado que los niveles de Lp (a) permanecen estables durante toda la vida fuera de la inflamación aguda, en la actualidad no hay mucho papel en la medición en serie de los niveles de Lp (a).
¿Cómo se trata? ¿Lp (a) elevado?
A pesar de las asociaciones observadas entre Lp (a) elevado y ASCVD, todavía no se ha realizado un ensayo controlado aleatorio para ver si la reducción dirigida de Lp (a) mejora los resultados clínicos. , se ha investigado el efecto de disminución de Lp (a) de las terapias disponibles actualmente.
De las terapias preventivas disponibles actualmente, solo un número limitado es eficaz para reducir la Lp (a).En el ensayo fundamental de evolocumab (FOURIER – Más resultados cardiovasculares investigados con inhibición de PCSK9 en sujetos con riesgo elevado), un inhibidor de PCSK9, Lp (a) se redujo en un 27% y la reducción observada en eventos cardiovasculares adversos mayores (MACE) fue mayor para aquellos con los niveles más altos de Lp (a) de referencia. De manera similar, alirocumab (en ODYSSEY OUTCOMES – Evaluación de los resultados cardiovasculares después de un síndrome coronario agudo durante el tratamiento con alirocumab) había aumentado la reducción de MACE en individuos con niveles basales más altos de Lp (a). Si bien estos resultados son alentadores, el impacto de los inhibidores de PCSK9 sobre Lp (a) es bastante modesto y se necesitan análisis adicionales antes de que los inhibidores de PCSK9 puedan recomendarse como terapia dirigida a Lp (a).
Se puede considerar la aféresis para pacientes seleccionados. Es muy eficaz para reducir los niveles de Lp (a), pero es un procedimiento costoso y engorroso para el que puede ser difícil obtener cobertura de seguro. Está reservado solo para los pacientes más refractarios y debe realizarse después de controlar de manera óptima los factores de riesgo conocidos con terapias probadas. En Alemania, la aféresis pareció producir una reducción del 70% en MACE en pacientes con eventos ASCVD recurrentes con Lp (a) elevado independientemente de los niveles de LDL-C.
Es importante destacar que varias estrategias preventivas de uso común son ineficaces. En particular, los cambios en el estilo de vida, incluidos la dieta y el ejercicio, no reducen la Lp (a). Los primeros datos sobre las estatinas mostraron resultados mixtos y algunos estudios sugirieron que incluso pueden conducir a aumentos de Lp (a). Sin embargo, estudios más contemporáneos muestran que la terapia con estatinas en sí misma afecta los niveles de Lp (a); aunque lo que es más importante, aquellos que continúan teniendo niveles altos de Lp (a) con una estatina tienen un mayor riesgo de ASCVD incluso si se mejora el LDL-C. La terapia de reemplazo hormonal reduce la Lp (a), pero su uso está limitado por el aumento excesivo de eventos adversos. La niacina reduce la Lp (a) un 23% pero no mejoró los resultados de ASCVD según los estudios AIM HIGH (niacina más estatina para prevenir eventos vasculares) y HPS2 THRIVE (tratamiento de HDL para reducir la incidencia de eventos vasculares). Aunque algunos la toleran, la niacina también se asocia con efectos secundarios importantes. Además, su eficacia es limitada en aquellos que pueden beneficiarse más (tamaño de isoforma pequeño y niveles basales de Lp más altos).
Según los datos disponibles, los autores recomiendan iniciar una terapia con estatinas de intensidad moderada a alta en adultos de 40 a 75 años con un riesgo de ASCVD a 10 años de 7.5% a ≤20% con un Lp (a) ≥100 nmol / L. Como ya se hace habitualmente, los pacientes de alto riesgo con LDL-C ≥70 mg / dL (no HDL-C ≥100 mg / dL) y una Lp (a) ≥100 nmol / L con estatina máxima tolerada deben considerarse durante más terapias intensivas (ezetimiba e inhibidores de PCSK9) para reducir el LDL-C.
Actualmente, se están estudiando nuevas terapias que se dirigen selectivamente a la Lp (a). Un ensayo de fase 2 de AKCEA apo (a) -LRx, un oligonucleótido antisentido de apo (a), redujo Lp (a) hasta un 80%. Se está planificando un estudio de fase 3. Además, un anticuerpo oxPL que se une e inactiva la actividad pro-osteogénica de Lp (a) tiene datos in vitro prometedores. Estas terapias, aunque prometedoras, requieren investigación adicional antes de convertirse en terapias convencionales.
Conclusión
La lipoproteína (a) representa un nuevo y emocionante biomarcador en el campo de la lipidología y la cardiología preventiva. La Lp (a) elevada está causalmente implicada en la ASCVD, y las pruebas en pacientes específicos pueden ayudar a adaptar la intensidad adecuada de las medidas preventivas. Sin embargo, debido a la falta de estandarización y heterogeneidad de los datos disponibles, los puntos de corte óptimos siguen siendo una fuente de intenso debate. El enfoque actual de la atención clínica es el control tradicional de los factores de riesgo en pacientes con Lp (a) alta, ya que las opciones de tratamiento dirigido son limitadas. Se están investigando activamente nuevas terapias dirigidas a Lp (a) y, si tienen éxito, podrían convertirse en un componente importante de la prevención primaria y secundaria.
Temas clínicos: Síndromes coronarios agudos, Diabetes y enfermedad cardiometabólica, Dislipidemia, Prevención, Enfermedad valvular del corazón , ACS y biomarcadores cardíacos, pruebas avanzadas de lípidos, hipercolesterolemia familiar homocigota, metabolismo de lípidos, no estatinas, nuevos agentes, hiperlipidemia primaria, estatinas, dieta
Palabras clave: dislipidemias, síndrome coronario agudo, American Heart Association, anticuerpos, monoclonal , Estenosis de la válvula aórtica, Apolipoproteínas A, Apolipoproteínas B, Eliminación de componentes sanguíneos, Isquemia cerebral, Marcadores biológicos, Enfermedades cardiovasculares, Colesterol, Química, Clínica, Constricción, Patológica, Comorbilidad, Dieta, Disulfuros, Toma de decisiones, Grupos étnicos, Fibrinólisis, Genoma- Estudio de asociación amplia, variación genética, terapia de reemplazo hormonal, inhibidores de hidroximetilglutaril-CoA reductasa, hipercolesterolemia, hiperlipoproteinemia tipo II, inflamación, patrones de herencia, estilo de vida, cobertura de seguro Antisentido, Antisentido, Estudios prospectivos, Fosfolípidos, Asignación aleatoria, Factores de riesgo, Evaluación de riesgos, Fosfolípidos, Asignación aleatoria, Factores de riesgo, Evaluación de riesgos, Antisentido, Edad, Lipoproteína (a), Lipoproteínas, LDL, Niacina, Oligonucleótidos, Organización Mundial de la Salud, Subtilisinas
< Volver a listados