Note de léditeur: Commentaire basé sur Wilson DP, Jacobson TA, Jones PH, et al. Utilisation de la lipoprotéine (a) en pratique clinique: un biomarqueur dont le temps est venu. Une déclaration scientifique de la National Lipid Association. J Clin Lipidol 2019; 13: 374-92.
Introduction
Le profil lipidique traditionnel a servi de pilier de lévaluation du risque de maladie cardiovasculaire athéroscléreuse (ASCVD) pendant des décennies. Cet outil est devenu encore plus important au fur et à mesure que des thérapies ciblées, telles que les statines et plus récemment les inhibiteurs de lézétimibe et de la proprotéine convertase subtilisine / kexine de type 9 (PCSK9), sont devenues disponibles. Même avec ces progrès dans la gestion des lipides, et plus largement dans le ciblage des facteurs de risque cardiovasculaires traditionnels, le risque persistant chez de nombreux patients indique la nécessité détudier dautres contributeurs comme cibles thérapeutiques possibles. La lipoprotéine (a) (Lp) est un biomarqueur prometteur pour aider à affiner stratégies actuelles dévaluation des risques ASCVD, et il est estimé être élevé dans environ 20% de la population mondiale. La recherche sur la Lp (a) suggère quelle a une valeur ajoutée en médecine préventive, et il est temps pour les cardiologues et les membres de léquipe cardiovasculaire denvisager de lutiliser régulièrement dans leur pratique. Sur la base des preuves de plus en plus nombreuses, Wilson et al ont récemment publié une directive sur lutilisation clinique de la Lp (a) de la National Lipid Association, et nous résumons ici les éléments clés de leur travail.
Quest-ce que la lipoprotéine (a) )?
La lipoprotéine (a) est une particule de lipoprotéine de basse densité (LDL) avec une apolipoprotéine ajoutée (a) (apo) attachée au composant apoplipoprotéine (b) (apo) de la particule LDL via un pont disulfure. La structure de Lp (a) est très hétérogène secondaire à de nombreuses isoformes différentes dapo (a) au sein de la population. Sur le plan étiologique, il peut avoir fourni un avantage de survie en aidant à la cicatrisation des plaies et en réduisant les saignements, en particulier lors de laccouchement. Le niveau de Lp (a) dun individu est de 80 à 90%, déterminé génétiquement selon un modèle dhérédité autosomique codominant avec une expression complète à lâge de 1 à 2 ans et des niveaux de type adulte atteints à environ 5 ans. En dehors des états inflammatoires aigus , le niveau de Lp (a) reste stable tout au long de la vie dun individu quel que soit son mode de vie.
Les premières données suggèrent un lien entre le niveau de Lp (a) et à la fois lASCVD et la sténose aortique valvulaire (EVA), mais le mécanisme physiopathologique exact nest pas entièrement clair. Une théorie actuelle inclut une contribution à deux volets de la molécule Lp (a). Apo (a) a une homologie avec le plasminogène et il a été démontré in vitro quil inhibe la fibrinolyse. Par conséquent, il pourrait hypothétiquement favoriser la thrombose au niveau des plaques artérielles vulnérables ou un écoulement turbulent dans la sténose provoquant une obstruction ou favorisant la formation demboles dans lEVA. La portion de type LDL peut favoriser le dépôt de cholestérol intimal, mais la teneur en cholestérol même à des niveaux très élevés de Lp (a) est inférieure aux seuils LDL traditionnels et contribue probablement moins. Des preuves plus récentes suggèrent que les phospholipides oxydés co-localisent avec les molécules de Lp (a) et, ensemble, peuvent favoriser un dysfonctionnement endothélial, une inflammation et une calcification dans le système vasculaire.
Des preuves de haute qualité soutiennent un lien entre les niveaux de Lp (a) et une variété de résultats cardiovasculaires. Une méta-analyse a montré un risque accru de maladie coronarienne et dinfarctus du myocarde avec des concentrations > 30 mg / dL (62 nmol / L) tandis que lessai INTERHEART a montré Lp (a) > 50 mg / dL était associé à un risque accru dinfarctus du myocarde (OR 1,48; IC à 95% 1,32-1,67; P < 0,001). La même méta-analyse a montré un risque accru daccident vasculaire cérébral à Lp (a) < 50 mg / dL et une autre a montré un risque 2x plus élevé dAVC ischémique avec des isoformes apo (a) plus petites. Le tableau 1 montre le risque de Lp (a) élevé sur une variété de conditions cardiovasculaires basées sur de grandes études prospectives, basées sur la population et que ces associations ont également été observées dans les études de randomisation mendéliennes. Enfin, des études dassociation pangénomique axées sur la variation génétique et le risque de maladie ont révélé que des concentrations élevées de Lp (a) confèrent le risque le plus élevé dASCVD et dEVA indépendamment dautres causes et facteurs de risque connus.
Tableau 1: Impact des niveaux élevés de Lp (a) sur divers résultats cliniques basés sur de grandes études prospectives basées sur la population et si ces conclusions étaient étayées par de grandes études de randomisation mendélienne.

Tableau 1

Tableau 1: Impact dune Lp élevée (a) ) sur divers résultats cliniques basés sur de grandes études prospectives basées sur la population et si ces conclusions étaient étayées par de grandes études de randomisation mendélienne.
Mesure et niveaux cibles de Lp (a)
Lun des principaux obstacles à lutilisation clinique de Lp (a) est que sa mesure et ses niveaux cibles nont pas été normalisés. Plusieurs dosages disponibles rapportent des résultats en masse (mg / dL) au lieu de concentration (nmol / L), cette dernière étant préférée. Contrairement à dautres lipides et lipoprotéines, la conversion directe entre ces deux unités nest pas possible en raison du nombre variable dunités répétées dans différentes isoformes dapo (a), ce qui conduit à une sur ou sous-estimation en fonction de la taille des particules. Indépendamment du test ou des unités utilisées, les niveaux de Lp (a) varient selon les groupes ethniques et les états pathologiques, ainsi que selon que les mesures provenaient déchantillons frais ou congelés, ce qui a rendu les niveaux cibles publiés incohérents. Heureusement, tous ces problèmes peuvent être surmontés par la standardisation du test et des mesures générées. La directive recommande de déclarer les niveaux de Lp (a) sous forme de concentration (nmol / L) à laide dun test calibré par rapport au manuel de référence secondaire de lOMS / Fédération internationale de chimie clinique et de médecine de laboratoire.
Sur la base des études disponibles, le La directive recommande un point de coupure universel de ≥ 100 nmol / L (environ ≥ 50 mg / dL), qui se rapproche du 80e percentile dans les populations américaines de race blanche. Cependant, lutilisation de ce point de coupure reste un sujet de débat parmi de nombreux experts de la communauté lipidique et cela découle probablement du manque de standardisation et de différences épidémiologiques. Cette controverse est représentée par les directives de 2018 de lAmerican Heart Association (ACC) / American Heart Association (AHA) sur le cholestérol, qui suggèrent que le risque élevé est ≥125 nmol / L (ou ≥50 mg / dL). Le seuil peut changer à mesure que des études supplémentaires sont terminées, sachant que le seuil peut varier en fonction du risque, de lorigine ethnique et des comorbidités.
Quels patients devraient faire mesurer la Lp (a)?
En supposant laccès à un test standardisé par lOMS, certains patients peuvent bénéficier du test de Lp (a) après une discussion de prise de décision partagée est terminé. Sur la base de cette directive, la mesure de la Lp (a) peut être raisonnable chez les patients ayant des antécédents personnels ou un parent au premier degré avec ASCVD prématurée (en particulier si autrement considéré à faible risque) et dans lhypercholestérolémie sévère (LDL-C ≥190 mg dL). Les tests chez ces patients peuvent déclencher une escalade du traitement, comme décrit ci-dessous. Des indications supplémentaires pour lesquelles les tests peuvent être raisonnables sont énumérées dans le tableau 2, notamment les patients dont la réponse LDL-C aux statines est inférieure à celle prévue, ou chez les patients à risque limite (5% à ≤ 7,5% de risque ASCVD à 10 ans) qui sont particulièrement intéressés à réduire leur risque ASCVD.
Tableau 2: Populations pour lesquelles les tests Lp (a) peuvent être raisonnables sur la base des preuves actuelles.
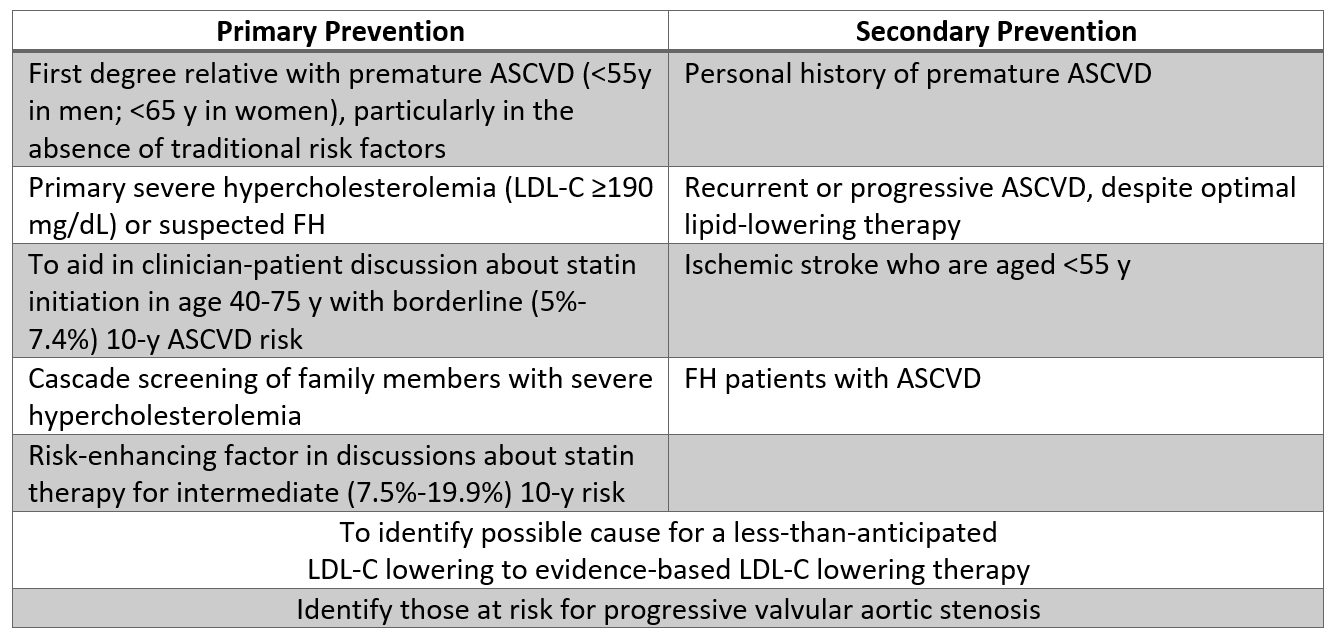
Tableau 2

Tableau 2: Populations pour lesquelles les tests Lp (a) peuvent être raisonnables sur la base des preuves actuelles.
Des études comme une sous-analyse JUPITER (Justification for Use of Statins in Prevention: An Intervention Trial Evaluating Rosuvastatin) montrent la Lp (a) est un bon prédicteur du risque lorsquil reste élevé chez les patients déjà sous statine. Cependant, aucune donnée disponible ne confirme que le traitement de la Lp (a) isolée et élevée conduit à de meilleurs résultats cliniques. Si et quand un traitement ciblé contre la Lp (a) devient disponible, il peut être raisonnable de commencer le dépistage universel à un jeune âge pour déterminer si des mesures préventives plus précoces sont indiquées.
Fait intéressant, il peut y avoir un effet plus aigu car les preuves actuelles montrent un lien entre une Lp élevée (a) et un AVC ischémique chez les jeunes. Par conséquent, il peut être raisonnable de mesurer la Lp (a) chez les jeunes présentant une hypercholestérolémie familiale (FH) génétiquement confirmée ou cliniquement suspectée, des antécédents familiaux de parent au premier degré avec ASCVD prématurée, ou un AVC ischémique ou un parent / frère dont la Lp est élevée. (une). Cependant, étant donné que les niveaux de Lp (a) restent stables tout au long de la vie en dehors de linflammation aiguë, il ny a pas beaucoup de mesure en série des niveaux de Lp (a) à lheure actuelle.
Comment traitez-vous Lp (a) élevée?
Malgré les associations observées entre une Lp (a) élevée et lASCVD, il ny a pas encore dessai contrôlé randomisé pour voir si une réduction ciblée de la Lp (a) améliore les résultats cliniques. Cependant , leffet de réduction de la Lp (a) des thérapies actuellement disponibles a été étudié.
Parmi les thérapies préventives actuellement disponibles, seul un nombre limité est efficace pour réduire la Lp (a).Dans lessai pivot dévolocumab (FOURIER – Autres résultats cardiovasculaires recherchés avec linhibition de la PCSK9 chez des sujets à risque élevé), un inhibiteur de la PCSK9, la Lp (a), a été réduit de 27% et la réduction observée des événements cardiovasculaires majeurs (MACE) était la plus élevée. pour ceux avec les niveaux de base de Lp (a) les plus élevés. De même, lalirocumab (dans ODYSSEY OUTCOMES – Evaluation of Cardiovascular Outcomes After and Acute Coronary Syndrome during Treatment With Alirocumab) a augmenté la réduction de la MACE chez les personnes ayant des taux de Lp (a) de base plus élevés. Bien que ces résultats soient encourageants, limpact des inhibiteurs de la PCSK9 sur la Lp (a) est assez modeste, et une analyse supplémentaire est nécessaire avant que les inhibiteurs de la PCSK9 puissent être recommandés comme thérapie ciblée sur la Lp (a).
Laphérèse peut être envisagée pour certains patients. Il est très efficace pour abaisser les niveaux de Lp (a), mais il sagit dune procédure coûteuse et lourde qui peut être difficile à obtenir une couverture dassurance. Elle est réservée aux seuls patients les plus réfractaires et doit être poursuivie après un contrôle optimal des facteurs de risque connus avec des thérapies éprouvées. En Allemagne, laphérèse a semblé entraîner une réduction de 70% de la MACE chez les patients présentant des événements ASCVD récurrents avec une Lp (a) élevée, indépendamment des taux de LDL-C.
Fait important, un certain nombre de stratégies préventives couramment utilisées sont inefficaces. Plus particulièrement, les changements de mode de vie, y compris le régime alimentaire et lexercice, ne réduisent pas la Lp (a). Les premières données sur les statines ont montré des résultats mitigés, certaines études suggérant quelles pourraient même conduire à des augmentations de la Lp (a). Cependant, des études plus contemporaines montrent que la thérapie par statine en elle-même affecte les niveaux de Lp (a); bien quimportant, ceux qui continuent à avoir des niveaux élevés de Lp (a) sur une statine courent un risque accru dASCVD même si le LDL-C est amélioré. Lhormonothérapie substitutive réduit la Lp (a), mais son utilisation est limitée par laugmentation excessive des événements indésirables. La niacine réduit la Lp (a) de 23% mais na pas amélioré les résultats de lASCVD sur la base des études AIM HIGH (Niacin Plus Statin to Prevent Vascular Events) et HPS2 THRIVE (Treatment of HDL to Reduce the Incidence of Vascular Events). Bien que tolérée par certains, la niacine est également associée à des effets secondaires importants. De plus, son efficacité est limitée chez ceux qui pourraient en bénéficier le plus (petite taille disoforme et niveaux de Lp de base les plus élevés).
Sur la base des données disponibles, les auteurs recommandent dinitier un traitement par statine dintensité modérée à élevée chez les adultes âgés de 40 à 75 ans avec un risque ASCVD à 10 ans de 7,5% à ≤ 20% avec une Lp (a) ≥ 100 nmol / L. Comme cela est déjà fait couramment, les patients à haut risque avec LDL-C ≥70 mg / dL (non-HDL-C ≥100 mg / dL) et une Lp (a) ≥100 nmol / L sous statine tolérée au maximum doivent être envisagés pour plus thérapies intensives (inhibiteurs dézétimibe et PCSK9) pour abaisser le LDL-C.
Actuellement, de nouvelles thérapies ciblant sélectivement la Lp (a) sont à létude. Un essai de phase 2 dAKCEA apo (a) -LRx, un oligonucléotide antisens apo (a), a réduit la Lp (a) jusquà 80%. Une étude de phase 3 est en cours de planification. De plus, un anticorps oxPL qui se lie et inactive lactivité pro-ostéogénique de Lp (a) a des données in vitro prometteuses. Ces thérapies, bien que prometteuses, nécessitent des recherches supplémentaires avant de devenir des thérapies courantes.
Conclusion
La lipoprotéine (a) représente un nouveau biomarqueur passionnant dans le domaine de la lipidologie et de la cardiologie préventive. Une Lp élevée (a) est causalement impliquée dans lASCVD, et des tests chez des patients spécifiques peuvent aider à adapter lintensité appropriée des mesures préventives. Cependant, en raison du manque de standardisation et de lhétérogénéité des données disponibles, les seuils optimaux restent une source de débats intenses. Les soins cliniques se concentrent actuellement sur le contrôle traditionnel des facteurs de risque chez les patients ayant une Lp (a) élevée, car les options de traitement ciblées sont limitées. De nouvelles thérapies ciblant la Lp (a) sont activement étudiées et, si elles réussissent, elles pourraient devenir un élément important de la prévention primaire et secondaire.
Thèmes cliniques: syndromes coronariens aigus, diabète et maladies cardio-métaboliques, dyslipidémie, prévention, cardiopathie valvulaire , ACS et biomarqueurs cardiaques, test lipidique avancé, hypercholestérolémie familiale homozygote, métabolisme lipidique, nonstatines, nouveaux agents, hyperlipidémie primaire, statines, régime alimentaire
Mots clés: dyslipidémie, syndrome coronarien aigu, American Heart Association, anticorps, monoclonaux , Sténose de la valve aortique, Apolipoprotéines A, Apolipoprotéines B, Élimination des composants sanguins, Ischémie cérébrale, Marqueurs biologiques, Maladies cardiovasculaires, Cholestérol, Chimie, Clinique, Constriction, Pathologique, Comorbidité, Alimentation, Disulfures, Prise de décision, Groupes ethniques, Fibrinolyse, Génome- Étude dassociation large, variation génétique, thérapie de remplacement dhormone, inhibiteurs de lhydroxyméthylglutaryl-CoA réductase, hypercholestérolémie, hyperlipoprotéinémie de type II, inflammation, modèles dhéritage, style de vie, couverture dassurance Âge, Lipoprotéine (a), Lipoprotéines, LDL, Niacine, Oligonucléotides, Antisens, Taille des particules, Phospholipides, Plasminogène, Études prospectives, Isoformes de protéines, Allocation aléatoire, Facteurs de risque, Évaluation des risques, Prévention secondaire, AVC, Thrombose, Organisation mondiale de la Santé, Subtilisines
< Retour aux listes