Anmerkung des Herausgebers: Kommentar basierend auf Wilson DP, Jacobson TA, Jones PH, et al. Verwendung von Lipoprotein (a) in der klinischen Praxis: ein Biomarker, dessen Zeit gekommen ist. Eine wissenschaftliche Stellungnahme der National Lipid Association. J Clin Lipidol 2019; 13: 374-92.
Einführung
Das traditionelle Lipidprofil Dieses Instrument dient seit Jahrzehnten als Hauptstütze für die Risikobewertung von atherosklerotischen Herz-Kreislauf-Erkrankungen (ASCVD). Dieses Instrument wurde noch wichtiger, als gezielte Therapien wie Statine und in jüngerer Zeit Ezetimib- und Proproteinkonvertase-Subtilisin / Kexin-Typ-9-Hemmer (PCSK9) verfügbar wurden. Trotz dieser Fortschritte beim Lipidmanagement und allgemeiner bei der Behandlung traditioneller kardiovaskulärer Risikofaktoren weist das anhaltende Risiko bei vielen Patienten auf die Notwendigkeit hin, andere Mitwirkende als mögliche therapeutische Ziele zu untersuchen. Lipoprotein (a) (Lp) ist ein vielversprechender Biomarker zur Verfeinerung aktuelle Strategien der ASCVD-Risikobewertung, und das ist es auch Schätzungen zufolge in etwa 20% der Weltbevölkerung erhöht. Untersuchungen zu Lp (a) legen nahe, dass es in der Präventivmedizin einen Mehrwert hat, und es ist Zeit für Kardiologen und Mitglieder des Herz-Kreislauf-Teams, darüber nachzudenken, es routinemäßig in ihrer Praxis anzuwenden. Basierend auf den zunehmenden Beweisen haben Wilson et al. Kürzlich eine Richtlinie zur klinischen Verwendung von Lp (a) von der National Lipid Association veröffentlicht, und hier fassen wir Schlüsselelemente ihrer Arbeit zusammen.
Was ist Lipoprotein (a )?
Lipoprotein (a) ist ein Lipoproteinpartikel niedriger Dichte (LDL) mit einem zugesetzten Apolipoprotein (a) (apo), das über a an die Apoplipoprotein (b) (apo) -Komponente des LDL-Partikels gebunden ist Disulfidbrücke. Die Struktur von Lp (a) ist sekundär zu vielen verschiedenen Apo (a) -Isoformen innerhalb der Population sehr heterogen. Ätiologisch kann es einen Überlebensvorteil gebracht haben, indem es die Wundheilung unterstützt und Blutungen reduziert, insbesondere bei der Geburt. Der Lp (a) -Wert eines Individuums ist zu 80-90% genetisch bestimmt in einem autosomalen codominanten Vererbungsmuster mit vollständiger Expression im Alter von 1-2 Jahren und erwachsenenähnlichen Niveaus im Alter von ungefähr 5 Jahren. Außerhalb akuter Entzündungszustände Das Lp (a) -Niveau bleibt während des gesamten Lebens eines Individuums unabhängig vom Lebensstil stabil.
Frühe Daten deuten auf einen Zusammenhang zwischen dem Lp (a) -Niveau und sowohl der ASCVD- als auch der Aortenstenose (VAS) hin, aber der genaue pathophysiologische Mechanismus ist nicht ganz klar. Eine aktuelle Theorie beinhaltet einen zweigleisigen Beitrag des Lp (a) -Moleküls. Apo (a) weist eine Homologie mit Plasminogen auf und es wurde in vitro gezeigt, dass es die Fibrinolyse hemmt. Daher könnte es hypothetisch die Thrombose an gefährdeten arteriellen Plaques oder den turbulenten Fluss innerhalb der Stenose fördern, was zu einer Obstruktion oder zur Förderung der Emboliebildung bei VAS führt. Der LDL-ähnliche Anteil kann die Ablagerung von intimem Cholesterin fördern, aber der Cholesteringehalt in selbst sehr hohen Lp (a) -Niveaus liegt unter den herkömmlichen LDL-Grenzwerten und trägt wahrscheinlich weniger dazu bei. Neuere Erkenntnisse deuten darauf hin, dass oxidierte Phospholipide zusammen mit Lp (a) -Molekülen lokalisiert sind und zusammen die endotheliale Dysfunktion, Entzündung und Verkalkung im Gefäßsystem fördern können.
Hochwertige Evidenz stützt einen Zusammenhang zwischen Lp (a) -Niveaus und einer Vielzahl von kardiovaskulären Ergebnissen. Eine Metaanalyse zeigte ein erhöhtes Risiko für KHK und MI mit Konzentrationen > 30 mg / dl (62 nmol / l), während die INTERHEART-Studie Lp (a) 50 mg / dl war mit einem erhöhten MI-Risiko verbunden (OR 1,48; 95% CI 1,32-1,67; P < 0,001). Dieselbe Metaanalyse zeigte ein erhöhtes Schlaganfallrisiko bei Lp (a) < 50 mg / dl und eine andere zeigte ein 2x höheres Risiko für einen ischämischen Schlaganfall mit kleineren Apo (a) -Isoformen. Tabelle 1 zeigt das Risiko eines erhöhten Lp (a) bei einer Vielzahl von kardiovaskulären Erkrankungen, basierend auf großen prospektiven, bevölkerungsbasierten Studien, und dass diese Assoziationen auch in Mendelschen Randomisierungsstudien beobachtet wurden. Genomweite Assoziationsstudien mit Schwerpunkt auf genetischer Variation und Krankheitsrisiko ergaben schließlich, dass hohe Lp (a) -Konzentrationen unabhängig von anderen bekannten Ursachen und Risikofaktoren das höchste Risiko für ASCVD und VAS bergen.
Tabelle 1: Einfluss erhöhter Lp (a) -Niveaus auf verschiedene klinische Ergebnisse basierend auf großen prospektiven, bevölkerungsbasierten Studien und ob diese Schlussfolgerungen durch große Mendelsche Randomisierungsstudien gestützt wurden.

Tabelle 1

Tabelle 1: Auswirkungen eines erhöhten Lp (a) ) Niveaus zu verschiedenen klinischen Ergebnissen basierend auf großen prospektiven, bevölkerungsbasierten Studien und ob diese Schlussfolgerungen durch große Mendelsche Randomisierungsstudien gestützt wurden.
Messung und Zielwerte von Lp (a)
Eines der Haupthindernisse für die klinische Anwendung von Lp (a) besteht darin, dass die Mess- und Zielwerte nicht standardisiert wurden. Mehrere verfügbare Assays geben Ergebnisse in Masse (mg / dl) anstelle von Konzentration (nmol / l) an, wobei letztere bevorzugt wird. Im Gegensatz zu anderen Lipiden und Lipoproteinen ist eine direkte Umwandlung zwischen diesen beiden Einheiten aufgrund der variablen Anzahl wiederholter Einheiten in verschiedenen Apo (a) -Isoformen nicht möglich, was je nach Partikelgröße zu einer Über- oder Unterschätzung führt. Unabhängig vom verwendeten Assay oder den verwendeten Einheiten variieren die Lp (a) -Niveaus zwischen ethnischen Gruppen und Krankheitszuständen sowie darüber, ob Messungen an frischen oder gefrorenen Proben durchgeführt wurden, wodurch veröffentlichte Zielwerte inkonsistent wurden. Glücklicherweise können all diese durch Standardisierung des Assays und generierte Messungen überwunden werden. In der Leitlinie wird empfohlen, die Lp (a) -Niveaus als Konzentration (nmol / l) unter Verwendung eines Assays anzugeben, der gegen das sekundäre Referenzhandbuch der WHO / Internationalen Föderation für klinische Chemie und Labormedizin kalibriert wurde.
Basierend auf den verfügbaren Studien wird die Die Richtlinie empfiehlt einen universellen Schnittpunkt von ≥ 100 nmol / l (ungefähr ≥ 50 mg / dl), der ungefähr dem 80. Perzentil in der kaukasischen US-Bevölkerung entspricht. Die Verwendung dieses Schnittpunkts bleibt jedoch unter vielen Experten in der Lipidgemeinschaft ein Thema der Debatte, und dies ist wahrscheinlich auf die mangelnde Standardisierung und die epidemiologischen Unterschiede zurückzuführen. Diese Kontroverse wird durch die Cholesterin-Richtlinien der American Heart Association (ACC) / American Heart Association (AHA) von 2018 dargestellt, die darauf hinweisen, dass ein hohes Risiko ≥ 125 nmol / l (oder ≥ 50 mg / dl) ist. Der Grenzwert kann sich ändern, wenn weitere Studien abgeschlossen sind, wobei berücksichtigt wird, dass der Grenzwert je nach Risiko, ethnischer Zugehörigkeit und Komorbidität variieren kann.
Bei welchen Patienten sollte Lp (a) gemessen werden?
Unter der Annahme, dass sie Zugang zu einem von der WHO standardisierten Assay haben, können ausgewählte Patienten nach einer gemeinsamen Entscheidungsdiskussion von Lp (a) -Tests profitieren abgeschlossen. Basierend auf dieser Richtlinie kann die Messung von Lp (a) bei Patienten mit einer persönlichen Vorgeschichte oder einem Verwandten ersten Grades mit vorzeitiger ASCVD (insbesondere wenn dies ansonsten als risikoarm angesehen wird) und bei schwerer Hypercholesterinämie (LDL-C ≥ 190 mg /) sinnvoll sein dL). Tests bei diesen Patienten können eine Eskalation der Therapie auslösen, wie nachstehend beschrieben. Zusätzliche Indikationen, bei denen Tests sinnvoll sein könnten, sind in Tabelle 2 aufgeführt, insbesondere bei Patienten, bei denen die LDL-C-Reaktion auf Statine geringer als erwartet ist, oder bei Patienten mit Borderline-Risiko (5% bis ≤ 7,5% 10-Jahres-ASCVD-Risiko), die sind besonders daran interessiert, ihr ASCVD-Risiko zu reduzieren.
Tabelle 2: Populationen, in denen Lp (a) -Tests nach aktuellen Erkenntnissen sinnvoll sein können.
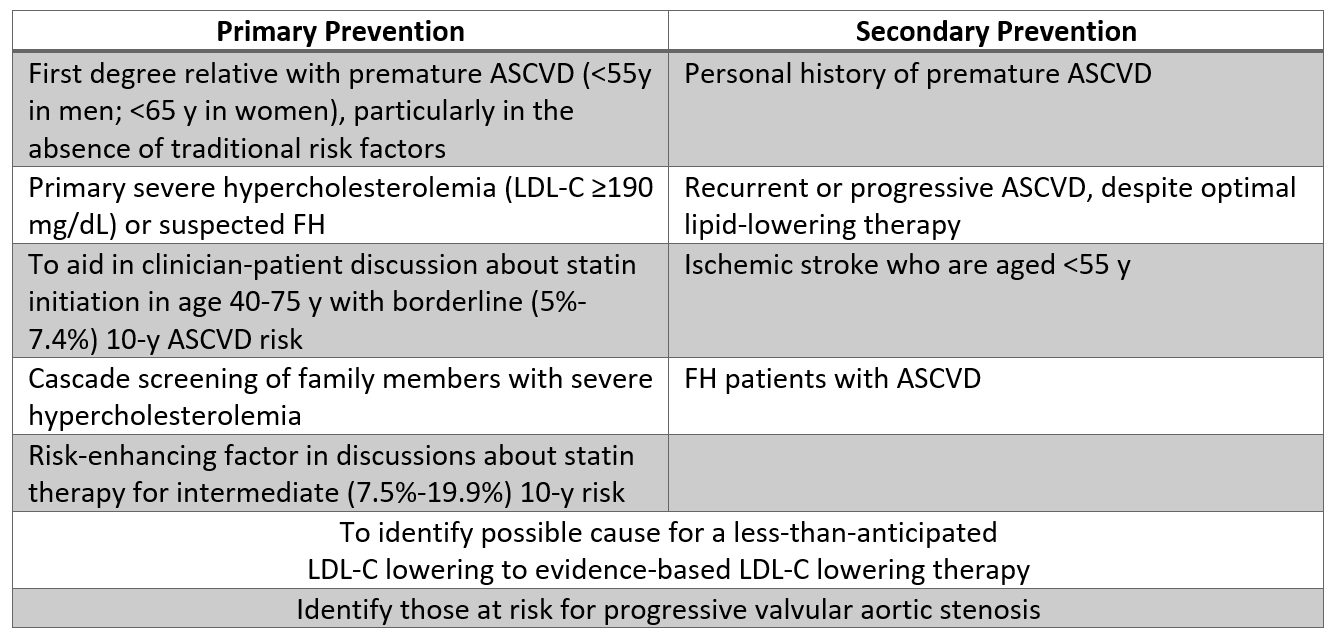
Tabelle 2

Tabelle 2: Populationen, in denen Lp (a) -Tests nach aktuellen Erkenntnissen sinnvoll sein können.
Studien wie eine JUPITER-Subanalyse (Begründung für die Verwendung von Statinen in der Prävention: Eine Interventionsstudie zur Bewertung von Rosuvastatin) zeigen Lp (a) ist ein starker Prädiktor für das Risiko, wenn es bei Patienten, die bereits ein Statin erhalten, erhöht bleibt. Es gibt jedoch keine verfügbaren Daten, die belegen, dass die Behandlung von isoliertem, erhöhtem Lp (a) zu besseren klinischen Ergebnissen führt. Wenn und wann eine gezielte Lp (a) -Behandlung verfügbar wird, kann es sinnvoll sein, bereits in jungen Jahren mit dem universellen Screening zu beginnen, um festzustellen, ob frühere vorbeugende Maßnahmen angezeigt sind.
Interessanterweise kann eine akutere Wirkung auftreten als Aktuelle Erkenntnisse zeigen einen Zusammenhang zwischen erhöhtem Lp (a) und ischämischem Schlaganfall in der Jugend. Daher kann es sinnvoll sein, Lp (a) bei Jugendlichen mit genetisch bestätigter oder klinisch vermuteter familiärer Hypercholesterinämie (FH), Familienanamnese ersten Grades mit vorzeitiger ASCVD oder ischämischem Schlaganfall oder einem Elternteil / Geschwister mit erhöhtem Lp zu messen (ein). Angesichts der Tatsache, dass die Lp (a) -Niveaus während des gesamten Lebens außerhalb einer akuten Entzündung stabil bleiben, spielt die serielle Messung der Lp (a) -Niveaus derzeit keine große Rolle.
Wie behandeln Sie sie? Erhöhtes Lp (a)?
Trotz der beobachteten Assoziationen zwischen erhöhtem Lp (a) und ASCVD muss noch eine randomisierte kontrollierte Studie durchgeführt werden, um festzustellen, ob eine gezielte Senkung von Lp (a) die klinischen Ergebnisse verbessert wurde die Lp (a) -senkende Wirkung derzeit verfügbarer Therapien untersucht.
Von den derzeit verfügbaren vorbeugenden Therapien ist nur eine begrenzte Anzahl bei der Reduzierung von Lp (a) wirksam.In der Zulassungsstudie mit Evolocumab (FOURIER – Weitere kardiovaskuläre Ergebnisse, die mit PCSK9-Hemmung bei Patienten mit erhöhtem Risiko untersucht wurden) wurde ein PCSK9-Inhibitor, Lp (a), um 27% reduziert, und die beobachtete Verringerung der schwerwiegenden unerwünschten kardiovaskulären Ereignisse (MACE) war am größten für diejenigen mit den höchsten Grundlinien-Lp (a) -Niveaus. In ähnlicher Weise hatte Alirocumab (in ODYSSEY OUTCOMES – Bewertung der kardiovaskulären Ergebnisse nach und des akuten Koronarsyndroms während der Behandlung mit Alirocumab) die MACE-Reduktion bei Personen mit höheren Lp (a) -Basiswerten erhöht. Obwohl diese Ergebnisse ermutigend sind, ist der Einfluss von PCSK9-Inhibitoren auf Lp (a) relativ gering, und es sind zusätzliche Analysen erforderlich, bevor PCSK9-Inhibitoren als auf Lp (a) ausgerichtete Therapie empfohlen werden können.
Apherese kann für ausgewählte Patienten in Betracht gezogen werden. Es ist sehr effektiv bei der Senkung des Lp (a) -Niveaus, aber ein kostspieliges und umständliches Verfahren, für das es schwierig sein kann, Versicherungsschutz zu erhalten. Es ist nur den refraktärsten Patienten vorbehalten und sollte nach optimaler Kontrolle bekannter Risikofaktoren mit bewährten Therapien fortgesetzt werden. In Deutschland schien die Apherese bei Patienten mit wiederkehrenden ASCVD-Ereignissen mit erhöhtem Lp (a) unabhängig von den LDL-C-Spiegeln zu einer 70% igen Verringerung der MACE zu führen.
Wichtig ist, dass eine Reihe häufig verwendeter Präventionsstrategien unwirksam sind. Vor allem Änderungen des Lebensstils, einschließlich Ernährung und Bewegung, reduzieren Lp (a) nicht. Frühe Daten zu Statinen zeigten gemischte Ergebnisse, wobei einige Studien darauf hinwiesen, dass sie sogar zu einem Anstieg von Lp (a) führen könnten. Zeitgemäßere Studien zeigen jedoch, dass die Statintherapie an sich die Lp (a) -Niveaus beeinflusst; Wichtig ist jedoch, dass diejenigen, die weiterhin hohe Lp (a) -Niveaus auf einem Statin aufweisen, ein erhöhtes ASCVD-Risiko haben, selbst wenn LDL-C verbessert wird. Die Hormonersatztherapie reduziert Lp (a), ihre Anwendung ist jedoch durch die übermäßige Zunahme unerwünschter Ereignisse begrenzt. Niacin reduziert Lp (a) um 23%, verbesserte jedoch nicht die ASCVD-Ergebnisse basierend auf den Studien AIM HIGH (Niacin Plus Statin zur Verhinderung von Gefäßereignissen) und HPS2 THRIVE (Behandlung von HDL zur Verringerung der Inzidenz von Gefäßereignissen). Während Niacin von einigen toleriert wird, ist es auch mit signifikanten Nebenwirkungen verbunden. Darüber hinaus ist seine Wirksamkeit bei denjenigen begrenzt, die am meisten davon profitieren können (kleine Isoformengröße und höchste Lp-Ausgangswerte).
Auf der Grundlage der verfügbaren Daten empfehlen die Autoren, eine Statintherapie mittlerer bis hoher Intensität einzuleiten bei Erwachsenen im Alter von 40 bis 75 Jahren mit einem 10-jährigen ASCVD-Risiko von 7,5% bis ≤ 20% mit einem Lp (a) ≥ 100 nmol / l. Wie bereits häufig üblich, sollten Hochrisikopatienten mit LDL-C ≥ 70 mg / dl (Nicht-HDL-C ≥ 100 mg / dl) und einem Lp (a) ≥ 100 nmol / l unter maximal toleriertem Statin für mehr in Betracht gezogen werden Intensive Therapien (Ezetimib- und PCSK9-Inhibitoren) zur Senkung von LDL-C.
Derzeit werden neuartige Therapien untersucht, die selektiv auf Lp (a) abzielen. Eine Phase-2-Studie mit AKCEA Apo (a) -LRx, einem Apo (a) Antisense-Oligonukleotid, reduzierte Lp (a) um bis zu 80%. Eine Phase-3-Studie ist in Planung. Zusätzlich weist ein oxPL-Antikörper, der die proosteogene Aktivität von Lp (a) bindet und inaktiviert, vielversprechende In-vitro-Daten auf. Diese Therapien sind zwar vielversprechend, erfordern jedoch zusätzliche Forschung, bevor sie zu Mainstream-Therapien werden.
Schlussfolgerung
Lipoprotein (a) ist ein aufregender neuer Biomarker auf dem Gebiet der Lipidologie und der präventiven Kardiologie. Erhöhtes Lp (a) ist kausal mit ASCVD verbunden, und Tests bei bestimmten Patienten können dazu beitragen, die angemessene Intensität vorbeugender Maßnahmen anzupassen. Aufgrund der mangelnden Standardisierung und Heterogenität der verfügbaren Daten bleiben optimale Grenzwerte jedoch eine Quelle intensiver Debatten. Der derzeitige Schwerpunkt der klinischen Versorgung liegt auf der traditionellen Risikofaktorkontrolle bei Patienten mit hohem Lp (a), da die gezielten Behandlungsmöglichkeiten begrenzt sind. Neuartige Lp (a) -Targeting-Therapien werden derzeit aktiv untersucht. Wenn sie erfolgreich sind, könnten sie zu einem wichtigen Bestandteil der Primär- und Sekundärprävention werden.
Klinische Themen: Akute Koronarsyndrome, Diabetes und kardiometabolische Erkrankungen, Dyslipidämie, Prävention, Herzklappenerkrankungen , ACS und kardiale Biomarker, fortgeschrittene Lipidtests, homozygote familiäre Hypercholesterinämie, Lipidstoffwechsel, Nichtstatine, neuartige Wirkstoffe, primäre Hyperlipidämie, Statine, Diät
Schlüsselwörter: Dyslipidämien, akutes Koronarsyndrom, American Heart Association, Antikörper, monoklonale , Aortenklappenstenose, Apolipoproteine A, Apolipoproteine B, Entfernung von Blutbestandteilen, Hirnischämie, biologische Marker, Herz-Kreislauf-Erkrankungen, Cholesterin, Chemie, klinisch, Verengung, pathologisch, Komorbidität, Ernährung, Disulfide, Entscheidungsfindung, ethnische Gruppen, Fibrinolyse, Genom- Breite Assoziationsstudie, genetische Variation, Hormonersatztherapie, Hydroxymethylglutaryl-CoA-Reduktase-Inhibitoren, Hypercholesterinämie, Hyperlipoproteinämie Typ II, Entzündung, Vererbungsmuster, Lebensstil, Versicherungsschutz Alter, Lipoprotein (a), Lipoproteine, LDL, Niacin, Oligonukleotide, Antisense, Partikelgröße, Phospholipide, Plasminogen, prospektive Studien, Proteinisoformen, zufällige Zuordnung, Risikofaktoren, Risikobewertung, Sekundärprävention, Schlaganfall, Thrombose, Weltgesundheitsorganisation, Subtilisine
< Zurück zu den Auflistungen