Vandets overfladespænding er ca. 72 mN / m ved stuetemperatur, hvilket er en af de højeste overfladespændinger for væske. Der er kun en væske med højere overfladespænding, og det er kviksølv, som er et flydende metal med en overfladespænding på næsten 500 mN / m. Hvorfor overfladespænding af kviksølv er så høj, vil også være tydelig efter at have læst dette korte blogindlæg.
Vandets høje overfladespænding er forårsaget af stærke molekylære interaktioner
Overfladespændingen opstår til sammenhængende interaktioner mellem molekylerne i væsken. På størstedelen af væsken har molekylerne nærliggende molekyler på hver side. Molekyler trækker hinanden ens i alle retninger og forårsager en nettokraft på nul. Imidlertid ved grænsefladen har de flydende molekyler kun halvdelen af de tilstødende flydende molekyler sammenlignet med hovedparten af væsken. Dette får molekylet til at forbinde sig stærkere med molekylerne på dets sider og forårsager en netto indadgående kraft mod væsken. Denne kraft modstår overfladebruddet og kaldes overfladespænding.
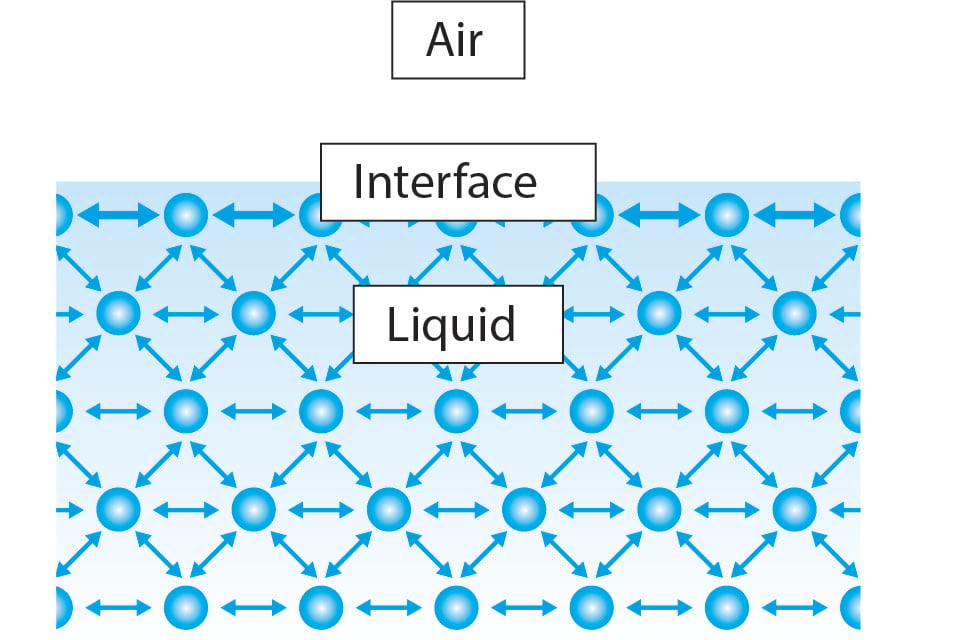
Med denne forklaring i tankerne er det så klart, at alle væsker vil have den samme egenskab, men hvorfor overfladespændingen af vand er meget højere end for eksempel ethanol.
For at forstå dette er vi nødt til at tænke på bindingerne mellem molekylerne. Som forklaret forårsager den sammenhængende kraft mellem molekylerne overfladespænding. Jo stærkere den sammenhængende kraft er, desto stærkere er overfladespændingen. Vandmolekylet har to hydrogenatomer bundet til et iltatom gennem kovalent binding. På grund af den høje elektronegativitet af ilt vil den have en stor del af den negative ladning på sin side, mens brint vil være mere positivt ladet. Dette forårsager en elektrostatisk tiltrækning mellem hydrogenatomet i et molekyle og oxygenatom i et andet. Dannede bindinger kaldes hydrogenbindinger, hvilket fører til stærke sammenhængskræfter mellem vandmolekylerne og høj overfladespænding af vand.
Som nævnt i begyndelsen af bloggen forklarer dette også, hvorfor kviksølv har så høj overfladespænding. Da kviksølv er et metal, er bindingerne mellem molekylerne metalbindinger, der er meget stærkere end hydrogenbindingerne, hvilket fører til meget høje sammenhængskræfter og høj overfladespænding.
At lære mere om vigtigheden af overfladespænding gennem linket nedenfor
